题目内容
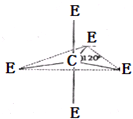 已知:A、B、C、D、E、M六种元素,原子序数依次增大.A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同;B是短周期中原子半径最大的主族元素;C元素基态原子核外的3p能级半充满;E是所在周期中电负性最大的元素;M是第四周期未成对电子最多的元素.试回答下列有关的问题:
已知:A、B、C、D、E、M六种元素,原子序数依次增大.A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同;B是短周期中原子半径最大的主族元素;C元素基态原子核外的3p能级半充满;E是所在周期中电负性最大的元素;M是第四周期未成对电子最多的元素.试回答下列有关的问题:(1)写出M元素基态原子核外电子排布式.写出含+6价M元素的一种常见钾盐的化学式.
(2)B、C、D、E的第一电离能由大到小的顺序是
(3)己知C、E两种元素组成的化合物通常有CE3、CE5两种.化合物CE3分子的空间构型是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同,则A为碳元素,B是短周期中原子半径最大的主族元素,则B是钠元素,C元素基态原子核外的3p能级半充满,则C为磷元素,M是第四周期未成对电子最多的元素,则M为铬元素,有6个未成对的电子,E是所在周期中电负性最大的元素,则E元素在第ⅤⅡA族,由于E的原子序数大于磷元素,小于铬元素,所以E为氯元素,D的原子序数介于磷和氯之间,则D为硫元素,据此答题.
解答:
解:A原子核外电子分占3个不同能级,且每个能级上排布的电子数相同,则A为碳元素,B是短周期中原子半径最大的主族元素,则B是钠元素,C元素基态原子核外的3p能级半充满,则C为磷元素,M是第四周期未成对电子最多的元素,则M为铬元素,有6个未成对的电子,E是所在周期中电负性最大的元素,则E元素在第ⅤⅡA族,由于E的原子序数大于磷元素,小于铬元素,所以E为氯元素,D的原子序数介于磷和氯之间,则D为硫元素,
(1)M为铬元素,是24号元素,所以它的基态原子核外电子排布式为1s22s22p63s23p63d54s1或[Ar]3d54s1,含+6价铬的一种常见钾盐的化学式为K2CrO4或K2Cr2O7,
答:M元素基态原子核外电子排布式为:1s22s22p63s23p63d54s1或[Ar]3d54s1; 含+6价M元素的一种常见钾盐的化学式为:K2CrO4或K2Cr2O7;
(2)B、C、D、E分别为Na、P、S、Cl,根据元素周期律,同周期从左向右,元素第一电离能逐渐增大,但第ⅤA族由于处于半满状态,第一电离能高于相邻的主族的同周期元素,所以它们第一电离能顺序为P>Cl>S>Na,A是C元素,C22-的电子式为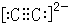 ,
,
故答案为:P>Cl>S>Na;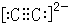 ;
;
(3)CE3为PCl3,分子的中心原子P的价层电子对数为
=4,所以P原子按sp3方式杂化,分子中有一对孤电子对,三个P-Cl键,所以PCl3的分子空间构型是三角锥形,CCl5分子中部分Cl换成Br原子,要使分子有三种可能的结构,则可以用2个Br或3个Br换Cl,即得到化学式为PBr2Cl3或PBr3Cl2,它们的相对分子质量分别为297.5或342,故答案为:三角锥形;sp3;297.5或342.
(1)M为铬元素,是24号元素,所以它的基态原子核外电子排布式为1s22s22p63s23p63d54s1或[Ar]3d54s1,含+6价铬的一种常见钾盐的化学式为K2CrO4或K2Cr2O7,
答:M元素基态原子核外电子排布式为:1s22s22p63s23p63d54s1或[Ar]3d54s1; 含+6价M元素的一种常见钾盐的化学式为:K2CrO4或K2Cr2O7;
(2)B、C、D、E分别为Na、P、S、Cl,根据元素周期律,同周期从左向右,元素第一电离能逐渐增大,但第ⅤA族由于处于半满状态,第一电离能高于相邻的主族的同周期元素,所以它们第一电离能顺序为P>Cl>S>Na,A是C元素,C22-的电子式为
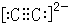 ,
,故答案为:P>Cl>S>Na;
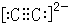 ;
;(3)CE3为PCl3,分子的中心原子P的价层电子对数为
| 5+3 |
| 2 |
点评:本题主要考查了原子核外电子排、第一电离能、同分异构体、电子式等知识点,中等难度,解题的关键在于根据原子结构特点推断元素.

练习册系列答案
相关题目
将等质量的铜片在酒精灯上加热后,分别插入下列溶液中,铜片质量增加的是( )
| A、硝酸 |
| B、稀盐酸 |
| C、Ca(OH)2溶液 |
| D、乙醇 |
用以下三种途径来制取相同质量的硝酸铜:
①铜与浓硝酸反应
②铜与稀硝酸反应
③铜与氧气反应生成CuO,CuO再与稀硝酸反应.
下列叙述中错误的是( )
①铜与浓硝酸反应
②铜与稀硝酸反应
③铜与氧气反应生成CuO,CuO再与稀硝酸反应.
下列叙述中错误的是( )
| A、消耗的硝酸的量:①>②>③ |
| B、铜与浓硝酸作用最快,故最佳方案是① |
| C、对环境造成的危害,③最小 |
| D、三种途径所消耗的铜的质量相等 |
已知HCN的电离常数Ka=5×10-10,H2CO3离常数Ka1=4.3×10-7、Ka2=5.6×10-11,判断在等浓度的NaCN、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| A、c(HCO3-)>c(CN- )>c(OH- ) |
| B、c(CN- )>c(HCO3-)>c(H+ ) |
| C、c(HCN)+c(CN- )=c(HCO3-)+c(H2CO3) |
| D、c(Na+ )+c(H+ )=c(HCO3- )+c(CN- )+C(OH- ) |
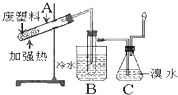 加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯,用图所示装置探究废旧塑料的再利用.下列叙述不正确的是( )
加热聚丙烯废塑料可以得到碳、氢气、甲烷、乙烯、丙烯、苯和甲苯,用图所示装置探究废旧塑料的再利用.下列叙述不正确的是( )| A、丙烯分子中共用电子对数为10 |
| B、装置B的试管中可收集到芳香烃 |
| C、装置C中的试剂可吸收烯烃以制取卤代烃 |
| D、最后收集的气体可做燃料 |
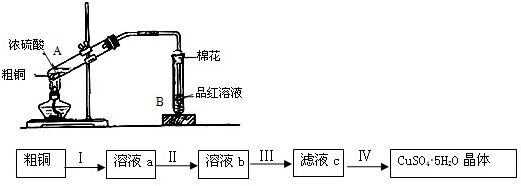
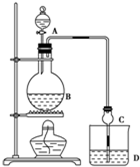 某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.
某课外小组设计的实验室制取乙酸乙酯的装置如图所示,A中放有浓硫酸,B中放有乙醇、无水醋酸钠,D中放有饱和碳酸钠溶液.