题目内容
12.1g N2中含有x个原子,则阿伏加德罗常数的值是( )| A. | $\frac{x}{28}$mol-1 | B. | $\frac{x}{14}$mol-1 | C. | 14x mol-1 | D. | 28x mol-1 |
分析 根据n=$\frac{m}{M}$计算氮气物质的量,氮原子物质的量为氮气的2倍,再根据N=nNA计算.
解答 解:1gN2物质的量为$\frac{1g}{28g/mol}$=$\frac{1}{28}$mol,
1g N2中含有x个原子,则$\frac{1}{28}$mol×2×NA=x,
解得NA=14x mol-1,
故选:C.
点评 本题考查阿伏加德罗常数、物质的量计算,掌握与物质的量为中心的计算.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
7.下列实验操作或记录正确的是( )
| A. | 用托盘天平称取2.50 g胆矾,受热充分失水后,固体质量减轻0.90g | |
| B. | 用量筒测得排水法收集制得的氢气体积为50.28mL | |
| C. | 用两只250 mL的容量瓶配制0.1mol•L-1500mLNaOH溶液 | |
| D. | 常温常压下测得1molN2的质量为28g |
17.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 6.72 L Cl2与足量的水反应转移的电子数为0.3NA | |
| B. | 1 mol Na被完全氧化生成Na2O2,失去2NA个电子 | |
| C. | 常温常压下,4.6g NO2和N2O4混合物中含有的原子总数为0.3NA | |
| D. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
4.下列措施不利于改善环境质量的是( )
| A. | 在燃煤中添加石灰石粉末 | B. | 用中和法除去工业废水中的酸 | ||
| C. | 随意地堆放生活垃圾 | D. | 在汽车上按照汽车尾气净化器 |
1.苯甲酸甲酯是一种重要的工业原料,有机化学中通过酯化反应原理,可以进行苯甲酸甲酯的合成.有关物质的物理性质、实验装置如下所示:
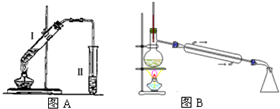
实验一:制取苯甲酸甲酯:在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验.
(1)苯甲酸与甲醇反应的化学方程式为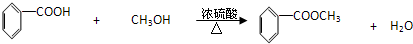 .
.
(2)大试管Ⅰ中除了装有15g苯甲酸和一定量的甲醇和沸石外还需要加入一定量浓硫酸,浓硫酸的作用是催化剂和吸水剂.
(3)实验室制取乙酸乙酯时,为了除去乙酸乙酯中混有的乙酸所用试剂为饱和碳酸钠溶液.
实验二:提纯苯甲酸甲酯:该实验要先把图A中制备的苯甲酸甲酯水洗提纯,再利用图B装置进行蒸馏提纯
(4)水洗提纯时所进行的操作为(填操作名称)分液.
(5)用图B装置进行蒸馏提纯时,当温度计显示199.6时,可用锥形瓶收集苯甲酸甲酯.
| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔点/℃ | 122.4 | -97 | -12.3 |
| 沸点/℃ | 249 | 64.3 | 199.6 |
| 密度/g.cm-3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

实验一:制取苯甲酸甲酯:在大试管中加入15g苯甲酸和一定量的甲醇,边振荡边缓慢加入一定量浓硫酸,按图A连接仪器并实验.
(1)苯甲酸与甲醇反应的化学方程式为
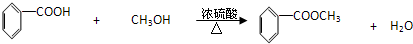 .
.(2)大试管Ⅰ中除了装有15g苯甲酸和一定量的甲醇和沸石外还需要加入一定量浓硫酸,浓硫酸的作用是催化剂和吸水剂.
(3)实验室制取乙酸乙酯时,为了除去乙酸乙酯中混有的乙酸所用试剂为饱和碳酸钠溶液.
实验二:提纯苯甲酸甲酯:该实验要先把图A中制备的苯甲酸甲酯水洗提纯,再利用图B装置进行蒸馏提纯
(4)水洗提纯时所进行的操作为(填操作名称)分液.
(5)用图B装置进行蒸馏提纯时,当温度计显示199.6时,可用锥形瓶收集苯甲酸甲酯.