题目内容
氢氧化钙的溶解度较小,20℃时,每100g水中共能溶解0.165g氢氧化钙.
(1)20℃时,在烧杯中放入7.40g氢氧化钙固体,加100g水,经充分搅拌后,所得饱和溶液的体积为100mL.计算溶液中OH-的物质的量浓度;
(2)在第(1)题所述的烧杯中需加入多少L物质的量浓度为0.1mol/L的Na2CO3溶液,才能使沉淀全部转化为CaCO3,使原溶液中的Ca2+离子浓度降至0.01mol/L?
(1)20℃时,在烧杯中放入7.40g氢氧化钙固体,加100g水,经充分搅拌后,所得饱和溶液的体积为100mL.计算溶液中OH-的物质的量浓度;
(2)在第(1)题所述的烧杯中需加入多少L物质的量浓度为0.1mol/L的Na2CO3溶液,才能使沉淀全部转化为CaCO3,使原溶液中的Ca2+离子浓度降至0.01mol/L?
考点:物质的量浓度的相关计算
专题:计算题
分析:(1)20℃时,每100g水中共能溶解0.165g氢氧化钙,则7.40g氢氧化钙固体,加100g水形成的溶液为饱和溶液,根据氢氧化钙的溶解度计算出溶液中氢氧根离子的物质的量浓度;
(2)反应前烧杯中含有的氢氧化钙为
=0.1mol,设出加入碳酸钠溶液的体积,然后根据反应后溶液中钙离子浓度计算出需要加入碳酸钠溶液的体积.
(2)反应前烧杯中含有的氢氧化钙为
| 7.40g |
| 74g/mol |
解答:
解:(1)由于20℃时,每100g水中共能溶解0.165g氢氧化钙,则在7.40g氢氧化钙固体中加100g水形成的溶液为饱和溶液,溶解的氢氧化钙的质量为0.165g,氢氧化钙的物质的量为:n=
=0.00223mol,则氢氧根离子的浓度为:c(OH-)=
=0.0446mol/L,
答:溶液中OH-的物质的量浓度为0.0446mol/L;
(2)设需要加入碳酸钠溶液的体积为xL,根据关系式Ca(OH)2~Na2CO3可知,加入的碳酸钠消耗的氢氧化钙的物质的量为:0.1xmol,反应前烧杯中氢氧化钙的物质的量为:
=0.1mol,
则:0.1mol-0.1xmol=0.01mol/L(0.1+x)L,
解得:x=0.9,
答:需要物质的量浓度为0.1mol/L的Na2CO3溶液的体积为0.9L.
| 0.165g |
| 74g/mol |
| 0.00223mol×2 |
| 0.1L |
答:溶液中OH-的物质的量浓度为0.0446mol/L;
(2)设需要加入碳酸钠溶液的体积为xL,根据关系式Ca(OH)2~Na2CO3可知,加入的碳酸钠消耗的氢氧化钙的物质的量为:0.1xmol,反应前烧杯中氢氧化钙的物质的量为:
| 7.40g |
| 74g/mol |
则:0.1mol-0.1xmol=0.01mol/L(0.1+x)L,
解得:x=0.9,
答:需要物质的量浓度为0.1mol/L的Na2CO3溶液的体积为0.9L.
点评:本题考查了物质的量浓度的计算、饱和溶液的性质,题目难度中等,注意掌握物质的量浓度的概念及计算方法,明确饱和溶液的特点为解答本题的关键,(1)为易错点,注意形成的溶液为饱和溶液.

练习册系列答案
相关题目
电浮选凝聚法处理酸性污水的工作原理如图.下列说法正确的是( )


| A、为增强污水的导电能力,可向污水中加入适量工业用食盐 |
| B、通入甲烷气体的电极反应式为:CH4-8e-+10OH-=CO32-+7H2O |
| C、若左池石墨电极产生22.4L气体,则消耗0.25 mol甲烷 |
| D、铁电极的电极反应式为:Fe-3e-=Fe3+ |
下列说法正确的是( )
| A、氧的摩尔质量是32 g?mol-1 |
| B、CO32-摩尔质量是60 g/mol |
| C、CO2的相对分子质量是44g |
| D、硫酸的摩尔质量是98g |
下列说法正确的是( )
A、
| ||||||||||
| B、11.7g食盐晶体中的分子数为0.2×6.02×10-23 | ||||||||||
| C、等量的白磷蒸气和白磷固体分别完全燃烧,后者放出热量多 | ||||||||||
| D、根据分散系的稳定性大小将混合物分为胶体、溶液和浊液 |
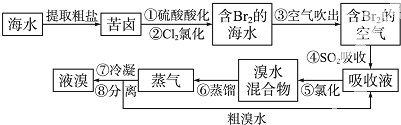
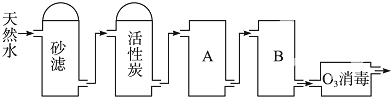
 (1)材料是人类赖以生存和发展的重要物质基础.
(1)材料是人类赖以生存和发展的重要物质基础.