题目内容
有一包白色粉末,含有Ba(NO3)2、CaCl2、K2CO3中的2种.为确定其成分,现做以下实验.结合资料卡片中的物质溶解性,试分析:
资料卡片:一些物质的溶解性
(1)将少量白色粉末加入足量水中,振荡,有白色沉淀生成.通过上述现象可初步判断原白色粉末中一定含有的物质是 (填化学式).
(2)过滤得到(1)中所产生的白色沉淀及滤液.实验室中进行过滤操作时,通常需要下列玻璃仪器中的 (填序号).
a.玻璃棒 b.普通漏斗 c.烧杯 d.容量瓶
(3)再继续向滤液中加入AgNO3溶液和过量稀硝酸,最终有白色沉淀生成.第(3)步实验及现象说明,原白色粉末中一定还含有的物质是 (填化学式),若将(2)中的白色沉淀溶于稀硝酸时,发生反应的化学方程式是 .
资料卡片:一些物质的溶解性
| OH- | CO | Cl- | NO | |
| Na+ | 溶 | 溶 | 溶 | 溶 |
| Ca2+ | 微 | 不 | 溶 | 溶 |
| Ba2+ | 溶 | 不 | 溶 | 溶 |
| Mg2+ | 不 | 微 | 溶 | 溶 |
(2)过滤得到(1)中所产生的白色沉淀及滤液.实验室中进行过滤操作时,通常需要下列玻璃仪器中的
a.玻璃棒 b.普通漏斗 c.烧杯 d.容量瓶
(3)再继续向滤液中加入AgNO3溶液和过量稀硝酸,最终有白色沉淀生成.第(3)步实验及现象说明,原白色粉末中一定还含有的物质是
考点:物质的检验和鉴别的实验方案设计
专题:实验设计题
分析:(1)由溶解性可知,少量白色粉末加入足量水中,振荡,有白色沉淀生成,白色沉淀为碳酸钡或碳酸钙;
(2)过滤需要烧杯、漏斗、玻璃棒;
(3)向滤液中加入AgNO3溶液和过量稀硝酸,最终有白色沉淀生成,白色沉淀为AgCl,以此来解答.
(2)过滤需要烧杯、漏斗、玻璃棒;
(3)向滤液中加入AgNO3溶液和过量稀硝酸,最终有白色沉淀生成,白色沉淀为AgCl,以此来解答.
解答:
解:(1)由溶解性可知,少量白色粉末加入足量水中,振荡,有白色沉淀生成,白色沉淀为碳酸钡或碳酸钙,则一定含K2CO3,故答案为:K2CO3;
(2)过滤需要烧杯、漏斗、玻璃棒,而容量瓶为配制溶液的仪器,故答案为:abc;
(3)向滤液中加入AgNO3溶液和过量稀硝酸,最终有白色沉淀生成,白色沉淀为AgCl,则原白色粉末中一定还含有的物质是CaCl2,(2)中的白色沉淀为CaCO3,与硝酸反应的化学反应为CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O,故答案为:CaCl2;CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O.
(2)过滤需要烧杯、漏斗、玻璃棒,而容量瓶为配制溶液的仪器,故答案为:abc;
(3)向滤液中加入AgNO3溶液和过量稀硝酸,最终有白色沉淀生成,白色沉淀为AgCl,则原白色粉末中一定还含有的物质是CaCl2,(2)中的白色沉淀为CaCO3,与硝酸反应的化学反应为CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O,故答案为:CaCl2;CaCO3+2HNO3=Ca(NO3)2+CO2↑+H2O.
点评:本题考查物质的检验和鉴别,为高频考点,把握物质的溶解性及白色沉淀的成分为解答的关键,侧重复分解反应及分析、应用能力的考查,题目难度不大.

练习册系列答案
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
在2L密闭容器中把4molA和2mol B混合,在一定条件下发生反应3A(g)+2B(g)?zC(g)+2D(g).2min后反应达到平衡时生成1.6mol C,又测得反应速率v(D)=0.2mol/(L?min).则下列说法正确的是( )
| A、z=4 | ||
| B、B物质的转化率是20% | ||
| C、A的平衡浓度是1.6 mol/L | ||
D、平衡时气体压强是原来的
|
关于下列实验的叙述合理的是( )
| A、某氢化物的溶液能使石蕊试液变蓝,该氢化物一定是氨气 |
| B、将某气体通入品红溶液中,品红溶液褪色,该气体一定是SO2 |
| C、配制硫酸亚铁溶液时应将硫酸亚铁固体溶于浓硫酸中,再稀释至所需浓度,以防止水解 |
| D、配制银氨溶液应将稀氨水逐滴滴入到硝酸银溶液中至产生的沉淀刚好溶解 |
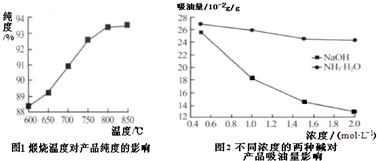
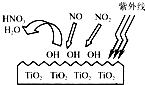 还原剂还原法、光催化氧化法、电化学吸收法是减少氮氧化物排放的有效措施.
还原剂还原法、光催化氧化法、电化学吸收法是减少氮氧化物排放的有效措施.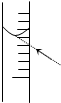 用18.4mol?L-1的浓H2SO4配制100mL浓度为1mol?L-1 H2SO4,其操作可分为以下几步:
用18.4mol?L-1的浓H2SO4配制100mL浓度为1mol?L-1 H2SO4,其操作可分为以下几步: