题目内容
9. 2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.
2SO2(g)+O2(g)?2SO3(g)反应过程的能量变化如图所示.已知1mol SO2(g)氧化为1mol SO3(g)的△H=-99kJ•mol-1.(1)该反应通常用V2O5作催化剂,加V2O5会使图中B点升高还是降低?降低,理由是使用催化剂能够降低反应的活化能;
(2)图中△H=-198kJ•mol-1;实验室在一定条件下,用4molSO2与足量的O2反应,当达到平衡时,放出198KJ热量时,则SO2的转化率为50%;
(3)已知单质硫的燃烧热为296kJ•mol-1,写出单质硫的燃烧热的热化学方程式S(s)+O2(g)?SO2(g)△H=-296kJ•mol-1.
分析 (1)使用催化剂能够降低反应的活化能;
(2)图中△H表示2molSO2(g)氧化为2molSO3放出的热量;
根据放出的热量计算参加反应二氧化硫物质的量,进而计算二氧化硫的转化率;
(3)燃烧热是1mol可燃物完全反应生成稳定氧化物放出的热量.
解答 解:(1)使用催化剂能够降低反应的活化能,加V2O5会使图中B点降低,
故答案为:降低;使用催化剂能够降低反应的活化能;
(2)因1mol SO2(g)氧化为1mol SO3的△H=-99kJ•mol-1,所以2molSO2(g)氧化为2molSO3的△H=-198kJ•mol-1;
达到平衡时,放出198KJ热量,则参加SO2的物质的量为2mol,则二氧化硫转化率为$\frac{2mol}{4mol}$×100%=50%;
故答案为:-198;50%;
(3)单质硫的燃烧热为296kJ•mol-1,单质硫的燃烧热的热化学方程式为:S(s)+O2(g)?SO2(g)△H=-296kJ•mol-1,
故答案为:S(s)+O2(g)?SO2(g)△H=-296kJ•mol-1.
点评 本题考查化学反应中能量变化、反应热计算、燃烧热、化学平衡计算等,难度不大,注意活化能与反应热的关系.

练习册系列答案
相关题目
13.在和铝反应能生成氢气的无色溶液中,下列各组离子可能大量共存的是( )
| A. | Cl-、Na+、NO3-、Ba2+ | B. | NH4+、HCO3-、Cl-、K+ | ||
| C. | K+、Ba2+、Cl-、SO42- | D. | Cu2+、NH4+、I-、Cl- |
17.把6mol A(g)和5mol B(g)混合后放入4L密闭容器中,在一定条件下发生反应,3A(气)+B(气)?2C(气)+xD(气),经过5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1 mol/(L•min),下列说法中错误的是( )
| A. | A的平均反应速率为0.15mol/(L•min) | |
| B. | 恒温达平衡时,容器内压强为开始时的75% | |
| C. | B的转化率为20% | |
| D. | 平衡时A的浓度为0.75mol/L |
4.在密闭容器中将1mol CO和5mol水蒸气的混合物加热到800℃时,有下列平衡:CO(g)+H2O(g)?CO2(g)+H2(g),且K=1.若用2mol CO和10mol H2O相互混合并加热到800℃,则CO的转化率为( )
| A. | 16.7% | B. | 50% | C. | 66.7% | D. | 83.3% |
1.下列分离方法中,正确的是( )
| A. | 将碘晶体中含有的少量沙子除去采用蒸馏的方法 | |
| B. | 蒸馏操作使用的温度计的水银球应插入到液体内 | |
| C. | 分离液体时,分液漏斗上的小孔与大气相通时打开活塞 | |
| D. | 若分液时不小心有少量上层液体流下来,补救措施是用滴管将其从烧杯中吸出 |
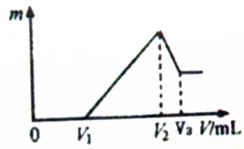 将0.1mol的镁、铝混合物溶于2mol/L H2SO4溶液中,然后再滴加0.1mol/L NaOH溶液.请回答:
将0.1mol的镁、铝混合物溶于2mol/L H2SO4溶液中,然后再滴加0.1mol/L NaOH溶液.请回答: