题目内容
无色难溶于水的气体是( )
| A、SO2 |
| B、NO |
| C、Cl2 |
| D、NO2 |
考点:氮的氧化物的性质及其对环境的影响,氯气的化学性质,二氧化硫的化学性质
专题:元素及其化合物
分析:A.SO2是无色、易难溶于水的气体;
B.NO是无色、难溶于水的气体;
C.氯气是黄绿色气体;
D.二氧化氮是红棕色气体有毒气体,能和水反应;
B.NO是无色、难溶于水的气体;
C.氯气是黄绿色气体;
D.二氧化氮是红棕色气体有毒气体,能和水反应;
解答:
解:A.SO2是无色、易溶于水的气体,故A不符合;
B.NO是无色、难溶于水的气体,故B符合;
C.氯气是黄绿色气体,1体积水能溶解2体积氯气,故C不符合;
D.NO2是红棕色、有毒气体,能和水反应生成硝酸和NO,易溶于水,故D不符合;
故选B.
B.NO是无色、难溶于水的气体,故B符合;
C.氯气是黄绿色气体,1体积水能溶解2体积氯气,故C不符合;
D.NO2是红棕色、有毒气体,能和水反应生成硝酸和NO,易溶于水,故D不符合;
故选B.
点评:本题考查了常见气体的性质,根据气体的颜色、毒性、溶解性来分析解答即可,熟悉常见气体的性质,总结归纳、灵活运用,题目难度不大.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
| A、常温常压下,48g O3所含的氧原子数为 3NA |
| B、常温常压下,22.4 L氧气所含的原子数为 2NA |
| C、标准状况下,22.4L H2O含有的分子数为 NA |
| D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
向体积为VaL浓度为0.05mol?L-1CH3COOH溶液中加入体积为Vb L浓度为0.05mol?L-1KOH溶液,下列关系错误的是( )
| A、Va>Vb时:c (CH3COOH)+c (CH3COO-)>c (K+) |
| B、Va=Vb时:c (CH3COOH)+c (H+)=c (OH-) |
| C、Va<Vb时:c (CH3COO-)>c (K+)>c (OH-)>c (H+) |
| D、Va与Vb任意比时:c (K+)+c (H+)=c (OH-)+c (CH3COO-) |
下列有关工业生产的叙述正确的是( )
| A、接触法制硫酸中采用沸腾炉的目的是为了使硫磺或黄铁矿燃烧充分,提高原料的利用率 |
| B、合成氨生产过程中采用高温高压条件都是为了提高N2、H2的转化率 |
| C、硫酸工业中,在接触室安装热交换器是为了利用硫磺或黄铁矿燃烧时放出的热量 |
| D、在联合制碱法中,参与循环的物质有CO2和NH3 |
糕点包装中常见的脱氧剂组成为还原性铁粉、氯化钠、炭粉等,其脱氧原理与钢铁的吸氧腐蚀相同.下列分析正确的是( )
| A、脱氧过程是吸热反应,可降低温度,延长糕点保质期 |
| B、含2.24g铁粉的脱氧剂,理论上最多能吸收氧气672mL(标准状况) |
| C、脱氧过程中碳做原电池负极,电极反应为:2H2O+O2+4 e-=4OH- |
| D、脱氧过程中铁作原电池正极,电极反应为:Fe-2e-=Fe2+ |
工业炼铁是在高炉中进行的,高炉炼铁的主要反应是:①2C(焦炭)+O2(空气)=2CO;②Fe2O3+3CO=2Fe+3CO该炼铁工艺中,对焦炭的实际使用量要远远高于按照化学方程式计算所需其主要原因是:( )
| A、CO过量 |
| B、CO与铁矿石接触不充分 |
| C、炼铁高炉的高度不够 |
| D、CO与Fe2O3的反应有一定限度 |
已知H-H键的键能为436kJ/mol,Cl-Cl键的键能为243kJ/mol,H-Cl键的键能为431kJ/mol,则H2(g)+Cl2(g)═2HCl(g)的反应热(△H)等于( )
| A、862kJ/mol |
| B、183kJ/mol |
| C、-862kJ/mol |
| D、-183kJ/mol |
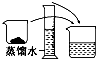
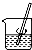
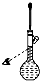
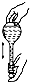
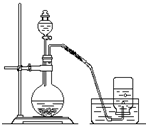 利用如图所示装置制取氧气并进行相关的实验探究.
利用如图所示装置制取氧气并进行相关的实验探究.