题目内容
下列有关溶液(常温下)中微粒浓度关系的叙述正确的是( )
| A、对于0.1 mol?L-1 Na2SO3溶液中:2c (Na+)═c(SO32-)+c(HSO3-)+c(H2SO3) |
| B、将CH3COOK溶液和盐酸溶液混合所得中性溶液:c(K+)>c(Cl-)=c(CH3COOH) |
| C、Ka(CH3COOH)=1.8×10-5,Ka(HCN)=4.9×10-10,物质的量浓度相同的CH3COONa、NaCN溶液中:c(CH3COO-)>c(CN-) |
| D、pH=11的氨水与pH=3的盐酸等体积混合:c(Cl-)=c(NH4+)>c(OH-)=c(H+) |
考点:离子浓度大小的比较
专题:盐类的水解专题
分析:A.根据亚硫酸钠溶液中的物料守恒判断;
B.根据电荷守恒c(K+)+c(H+)=c(Cl-)+c(OH-)+c(CH3COO-)和质子守恒c(Cl-)+c(OH-)=c(H+)+c(CH3COOH)进行分析;
C.酸根离子对应酸的酸性越强,酸根离子的水解程度越大,水解程度越大,则酸根离子浓度越小;
D.一水合氨为弱碱,混合液中氨水过量,溶液显示碱性,则c(OH-)>c(H+).
B.根据电荷守恒c(K+)+c(H+)=c(Cl-)+c(OH-)+c(CH3COO-)和质子守恒c(Cl-)+c(OH-)=c(H+)+c(CH3COOH)进行分析;
C.酸根离子对应酸的酸性越强,酸根离子的水解程度越大,水解程度越大,则酸根离子浓度越小;
D.一水合氨为弱碱,混合液中氨水过量,溶液显示碱性,则c(OH-)>c(H+).
解答:
解:A.对于0.1 mol?L-1 Na2SO3溶液中一定满足物料守恒:c (Na+)═2c(SO32-)+2c(HSO3-)+2c(H2SO3),故A错误;
B.混合液为中性,则c(OH-)=c(H+),根据电荷守恒c(K+)+c(H+)=c(Cl-)+c(OH-)+c(CH3COO-)可得:c(K+)=c(Cl-)+c(CH3COO-),所以c(K+)>c(Cl-);根据质子守恒可得:c(Cl-)+c(OH-)=c(H+)+c(CH3COOH),由于c(OH-)=c(H+),则c(Cl-)=c(CH3COOH),故B正确;
C.Ka(CH3COOH)=1.8×10-5,Ka(HCN)=4.9×10-10,则酸性:CH3COOH>HCN,则醋酸钠的水解程度小于NaCN,所以物质的量浓度相同的CH3COONa、NaCN溶液中:c(CH3COO-)>c(CN-),故C正确;
D.pH=11的氨水与pH=3的盐酸等体积混合,一水合氨为弱碱,氨水浓度大于盐酸,则混合液中氨水过量,溶液显示碱性,则c(OH-)>c(H+),根据电荷守恒可得:c(Cl-)<c(NH4+),溶液中正确的离子浓度大小为:c(NH4+)>c(Cl-)>c(OH-)>c(H+),故D错误;
故选BC.
B.混合液为中性,则c(OH-)=c(H+),根据电荷守恒c(K+)+c(H+)=c(Cl-)+c(OH-)+c(CH3COO-)可得:c(K+)=c(Cl-)+c(CH3COO-),所以c(K+)>c(Cl-);根据质子守恒可得:c(Cl-)+c(OH-)=c(H+)+c(CH3COOH),由于c(OH-)=c(H+),则c(Cl-)=c(CH3COOH),故B正确;
C.Ka(CH3COOH)=1.8×10-5,Ka(HCN)=4.9×10-10,则酸性:CH3COOH>HCN,则醋酸钠的水解程度小于NaCN,所以物质的量浓度相同的CH3COONa、NaCN溶液中:c(CH3COO-)>c(CN-),故C正确;
D.pH=11的氨水与pH=3的盐酸等体积混合,一水合氨为弱碱,氨水浓度大于盐酸,则混合液中氨水过量,溶液显示碱性,则c(OH-)>c(H+),根据电荷守恒可得:c(Cl-)<c(NH4+),溶液中正确的离子浓度大小为:c(NH4+)>c(Cl-)>c(OH-)>c(H+),故D错误;
故选BC.
点评:本题考查了溶液中离子浓度大小比较、酸碱混合的定性判断,题目难度中等,试题知识点较多,充分考查了学生对基础知识的把握情况,要求学生能够利用电荷守恒、物料守恒、质子守恒及盐的水解原理判断溶液中各离子浓度大小,选项D为易错点,注意混合液中氨水过量.

练习册系列答案
相关题目
下列说法中错误的有( )
①、容量瓶用蒸馏水洗净以后,还需要用待配溶液润洗
②、配制950mL 0.5mol?L-1 CuSO4 溶液应选用1000mL 容量瓶
③、定容时仰视刻度线将导致溶液体积偏大,浓度偏低
④、应在天平的左边放上滤纸称量NaOH固体,在右边放砝码
⑤、将烧杯中的溶液小心注入容量瓶后,然后加蒸馏水定容.
①、容量瓶用蒸馏水洗净以后,还需要用待配溶液润洗
②、配制950mL 0.5mol?L-1 CuSO4 溶液应选用1000mL 容量瓶
③、定容时仰视刻度线将导致溶液体积偏大,浓度偏低
④、应在天平的左边放上滤纸称量NaOH固体,在右边放砝码
⑤、将烧杯中的溶液小心注入容量瓶后,然后加蒸馏水定容.
| A、①②③ | B、①②⑤ |
| C、①④⑤ | D、③④⑤ |
药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:下列有关叙述正确的是( )
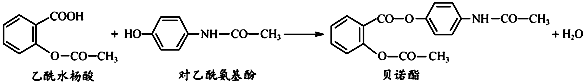

| A、乙酰水杨酸和对乙酰氨基酚均能与NaHCO3 溶液反应 |
| B、可用FeCl3 溶液区别乙酰水杨酸和贝诺酯 |
| C、贝诺酯分子中有2种含氧官能团 |
| D、贝诺酯与足量NaOH 溶液共热,生成乙酰水杨酸钠和对乙酰氨基酚钠 |
“秦砖汉瓦”是我国传统建筑文化的一个缩影.同是由黏土烧制的砖瓦,有的是黑色的,有的却是红色的,你猜测其中的原因可能( )
| A、土壤中含有铁粉、二氧化锰等 |
| B、黑砖瓦是煅烧过程中附着了炭黑,红砖则是添加了红色耐高温染料 |
| C、土壤中含有的铜元素经过不同工艺煅烧,分别生成了黑色CuO和红色Cu或Cu2O |
| D、土壤中含有的铁元素经过不同工艺煅烧,分别生成了黑色Fe304或FeO和红色Fe2O3 |
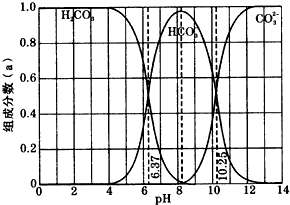 如图是一水溶液在pH从0到14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成分数,下列叙述正确的是( )
如图是一水溶液在pH从0到14的范围内,H2CO3、HCO3-、CO32-三种成分平衡时的组成分数,下列叙述正确的是( )| A、此图是1.0 mol/L碳酸钠溶液滴定1.0 mol/L HCl溶液的滴定曲线 |
| B、在pH为6.37及10.25时,溶液中c(H2CO3)=c(HCO3-)=c(CO32-) |
| C、人体血液的pH约为7.4,则CO2在血液中多以HCO3-的形式存在 |
| D、若用CO2和NaOH反应制取Na2CO3,溶液的pH必须控制在10以上 |
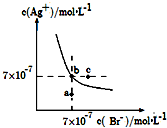 在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )
在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )| A、如图中a点对应的是AgBr的不饱和溶液 |
| B、在t℃时,Ksp(AgBr)=4.9×10-13 |
| C、在t℃时,AgCl(s)+Br-(aq)?AgBr(s)+Cl-(aq)的平衡常数K≈816 |
| D、在AgBr的饱和溶液中加入NaBr固体,可使溶液由b点到以c点 |
下列关于金属的叙述正确的是( )
| A、为解决当下能源紧却问题,可大力发展冶炼铝工业 |
| B、我国使用最早的合金是黄铜 |
| C、人类对镁的使用比铁更早,镁的合金具有质量轻、硬度较大的优点 |
| D、目前用量最大,使用最广的合金是钢 |
下列说法错误的是( )
| A、化学是在分子、原子水平上认识物质,了解化学可以改变分子、创造出新的分子 |
| B、医疗上所用“钡餐”使用的是氯化钡 |
| C、氮化硅陶瓷、通讯光缆等都是新型无机非金属材料 |
| D、盐卤能使蛋白质变性,因此喝不得,但可以用盐卤做豆腐 |
下列说法中正确的是( )
| A、在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B、化学反应中的能量变化都表现为热量变化 |
| C、△H的大小与热化学方程式的计量数无关 |
| D、生成物的总焓大于反应物的总焓时,反应吸热,△H>0 |