题目内容
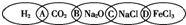 对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的.如图为一“链状连环”图案,图案上由左到右分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分由左到右A、B、C、D为其相应的分类依据代号.
对于数以千万计的化学物质和为数更多的化学反应,分类法的作用几乎是无可替代的.如图为一“链状连环”图案,图案上由左到右分别写了H2、CO2、Na2O、NaCl、FeCl3五种物质,图中相连的两种物质均可归属为一类,相交部分由左到右A、B、C、D为其相应的分类依据代号.请回答下列问题:
(1)请将分类依据代号填入相应的括号内.
(2)用洁净的烧杯取少量蒸馏水,用酒精灯加热至沸腾,向烧杯中逐滴加入1mol?L-1的图中一种化合物的水溶液,可制得一种红色胶体.
①反应的化学方程式为
②如何用较简单的方法判断胶体是否制备成功?
③向该胶体中逐滴加入HI稀溶液,先出现红褐色沉淀,随后红褐色沉淀溶解,此反应的离子方程式是
考点:酸、碱、盐、氧化物的概念及其相互联系,胶体的重要性质
专题:物质的分类专题,溶液和胶体专题
分析:(1)电解质是在水溶液中或熔融状态下能导电的化合物;
含有钠元素的化合物称为钠的化合物;
盐是阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物;
(2)①制备胶体的原理是利用铁离子水解生成氢氧化铁胶体;
②胶体有丁达尔效应:用一束光线照射,能产生一条光亮的通路;
③胶体遇电解质发生聚沉,生成的Fe(OH)3沉淀能与碘化氢发生中和反应;
含有钠元素的化合物称为钠的化合物;
盐是阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物;
(2)①制备胶体的原理是利用铁离子水解生成氢氧化铁胶体;
②胶体有丁达尔效应:用一束光线照射,能产生一条光亮的通路;
③胶体遇电解质发生聚沉,生成的Fe(OH)3沉淀能与碘化氢发生中和反应;
解答:
解:(1)电解质是在水溶液中或熔融状态下能导电的化合物,电解质包括酸、碱、盐、金属氧化物和水,故H2、CO2不是电解质;
含有钠元素的化合物称为钠的化合物,故Na2O、NaCl为钠的化合物;
盐是阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物,故NaCl、FeCl3为盐;
故答案为:H2、CO2;Na2O、NaCl;NaCl、FeCl3;
(2))①制备胶体的原理是利用铁离子水解生成氢氧化铁胶体,反应的化学方程式为FeCl3+3H2O
Fe(OH)3(胶体)+3HCl;
故答案为:FeCl3+3H2O
Fe(OH)3(胶体)+3HCl;
②溶液不产生丁达尔效应,而氢氧化铁胶体能产生丁达尔效应,
故答案为:若该分散系能产生丁达尔效应,则制备成功;否则,不成功;
③加入电解质后,Fe(OH)3胶体发生聚沉,随后沉淀溶解,溶液呈黄色,这是氢氧化铁被HI溶解所致,此反应的离子方程式为:2Fe(OH)3++2I-+6H+=2Fe2++I2+3H2O,故答案为:2Fe(OH)3++2I-+6H+=2Fe2++I2+3H2O;
含有钠元素的化合物称为钠的化合物,故Na2O、NaCl为钠的化合物;
盐是阳离子是金属离子或铵根离子,阴离子是酸根离子的化合物,故NaCl、FeCl3为盐;
故答案为:H2、CO2;Na2O、NaCl;NaCl、FeCl3;
(2))①制备胶体的原理是利用铁离子水解生成氢氧化铁胶体,反应的化学方程式为FeCl3+3H2O
| ||
故答案为:FeCl3+3H2O
| ||
②溶液不产生丁达尔效应,而氢氧化铁胶体能产生丁达尔效应,
故答案为:若该分散系能产生丁达尔效应,则制备成功;否则,不成功;
③加入电解质后,Fe(OH)3胶体发生聚沉,随后沉淀溶解,溶液呈黄色,这是氢氧化铁被HI溶解所致,此反应的离子方程式为:2Fe(OH)3++2I-+6H+=2Fe2++I2+3H2O,故答案为:2Fe(OH)3++2I-+6H+=2Fe2++I2+3H2O;
点评:本题考查胶体的性质和离子方程式的书写,题目难度不大,注意HI既有酸性又有强还原性,I-能使Fe(OH)3胶粒聚沉,H+使其溶解.

练习册系列答案
相关题目
下列说法正确的是( )
| A、13C和14C属于同一种元素,它们互为同位素 |
| B、1H和2H是不同的粒子,但它们的质子数相等 |
| C、14C 和14N的质量数相等,它们互为同位素 |
| D、6Li和7Li的电子数相等,但中子数不相等 |
烧碱的化学式为( )
| A、NaCl |
| B、NaOH |
| C、NaHCO3 |
| D、Na2CO3 |
当光束通过下列分散系时,可能产生丁达尔效应的是( )
| A、NaHCO3溶液 |
| B、蔗糖溶液 |
| C、CuSO4溶液 |
| D、Fe(OH)3胶体 |
铝可以制造多种建筑型材.铝在空气中能够稳定存在的原因是( )
| A、铝的活泼性很差 |
| B、铝的还原性很差 |
| C、铝与氧气不反应 |
| D、铝表面有致密的氧化膜 |
