题目内容
某兴趣小组同学共同设置了如图所示的实验装置,既可用于制取气体,又可用于验证物质的性质提供如下药品(KMnO4 固体;NaBr 溶液;CCI4;水;饱和食盐水;电石;溴水;浓盐酸)
已知:16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O
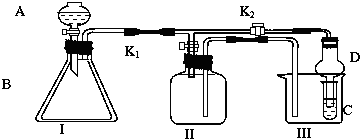
(1)利用I、II装置制取气体(K2闭,K1打开).甲同学认为:利用II装置可以收集H2、NH3 等气体,但不能收集O2 和NO 等气体,其理由是: 乙同学认为:利用II装置作简单改进,(不改变仪器装置),也可收集O2 和NO等气体,但不能收集NO2气体,改进的方法是 ,利用II装置再作简单改进(不改变仪器装置),还可收集NO2 气体,改进方法 .
(2)利用I、III装置验证物质的性质(K2打开,K1关闭)如设计证明氧化性:KMnO4>Cl2>Br2,则在A中加浓盐酸,C中加 ,观察到C中的现象是 .
(3)请利用I、III 装置自行设计有机实验,写出实验所用的试剂,简述C中的实验现象及根据此现象所得结论.B中加 C中的实验现象: .
已知:16HCl+2KMnO4=2KCl+2MnCl2+5Cl2↑+8H2O

(1)利用I、II装置制取气体(K2闭,K1打开).甲同学认为:利用II装置可以收集H2、NH3 等气体,但不能收集O2 和NO 等气体,其理由是:
(2)利用I、III装置验证物质的性质(K2打开,K1关闭)如设计证明氧化性:KMnO4>Cl2>Br2,则在A中加浓盐酸,C中加
(3)请利用I、III 装置自行设计有机实验,写出实验所用的试剂,简述C中的实验现象及根据此现象所得结论.B中加
考点:常见气体制备原理及装置选择
专题:常规题型,元素及其化合物
分析:(1)甲同学:根据气体的密度及性质选择收集方法;
乙同学:根据O2 和NO性质选择收集方法;根据二氧化氮的性质选择收集方法,注意不改变仪器装置,二氧化氮极易与水反应;
(2)根据氧化剂+还原剂=氧化产物+还原产物,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物,判断可能发生的反应,以及反应现象;
(3)用石灰石、醋酸、硅酸钠溶液等药品设计实验:比较碳酸、醋酸、硅酸的酸性强弱;根据强酸制弱酸,石灰石和醋酸反应生成二氧化碳,二氧化碳和硅酸钠反应生成硅酸沉淀,据此分析实验目的和现象.
乙同学:根据O2 和NO性质选择收集方法;根据二氧化氮的性质选择收集方法,注意不改变仪器装置,二氧化氮极易与水反应;
(2)根据氧化剂+还原剂=氧化产物+还原产物,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物,判断可能发生的反应,以及反应现象;
(3)用石灰石、醋酸、硅酸钠溶液等药品设计实验:比较碳酸、醋酸、硅酸的酸性强弱;根据强酸制弱酸,石灰石和醋酸反应生成二氧化碳,二氧化碳和硅酸钠反应生成硅酸沉淀,据此分析实验目的和现象.
解答:
解:(1)甲同学:O2的密度大于空气的密度,所以氧气应采用向上排空气法收集;一氧化氮和氧气能发生反应生成二氧化氮,一氧化氮应采用排水法收集,所以该装置不能收集氧气和一氧化氮;
乙同学:O2 和NO不能与水发生反应,而且难溶于水,所以能采用排水法收集;二氧化氮和水能发生反应,不能采用排水法收集,二氧化氮的密度大于空气的密度,所以应采用排难挥发的有机溶剂或向上排空气法收集;该装置不改变仪器装置,所以只能采用排难挥发的有机溶剂法收集;
故答案为:氧气的密度比空气的大,一氧化氮与空气的密度相差不大而且一氧化氮能和氧气反应生成二氧化氮;将装置Ⅱ中加满水;将装置Ⅱ中加满难挥发的有机溶剂;
(2)根据氧化剂+还原剂=氧化产物+还原产物,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物,证明氧化性:KMnO4>Cl2>Br2,可将KMnO4作为氧化剂和盐酸反应判断是否生成氯气,如氯气氧化性大于Br2,则将氯气通入NaBr溶液中,如果溶液变为橙红色,说明有Br2生成,从而确定氧化性:KMnO4>Cl2>Br2.
故答案为:溴化钠溶液;溶液呈橙色;
(3)石灰石和醋酸反应生成二氧化碳,二氧化碳和硅酸钠反应生成硅酸沉淀,所以B中固体溶解,产生无色气体,C试管中产生白色沉淀,实验的目的是比较碳酸、醋酸、硅酸的酸性强弱,
故答案为:石灰石;C试管中产生白色沉淀.
乙同学:O2 和NO不能与水发生反应,而且难溶于水,所以能采用排水法收集;二氧化氮和水能发生反应,不能采用排水法收集,二氧化氮的密度大于空气的密度,所以应采用排难挥发的有机溶剂或向上排空气法收集;该装置不改变仪器装置,所以只能采用排难挥发的有机溶剂法收集;
故答案为:氧气的密度比空气的大,一氧化氮与空气的密度相差不大而且一氧化氮能和氧气反应生成二氧化氮;将装置Ⅱ中加满水;将装置Ⅱ中加满难挥发的有机溶剂;
(2)根据氧化剂+还原剂=氧化产物+还原产物,氧化性:氧化剂>氧化产物,还原性:还原剂>还原产物,证明氧化性:KMnO4>Cl2>Br2,可将KMnO4作为氧化剂和盐酸反应判断是否生成氯气,如氯气氧化性大于Br2,则将氯气通入NaBr溶液中,如果溶液变为橙红色,说明有Br2生成,从而确定氧化性:KMnO4>Cl2>Br2.
故答案为:溴化钠溶液;溶液呈橙色;
(3)石灰石和醋酸反应生成二氧化碳,二氧化碳和硅酸钠反应生成硅酸沉淀,所以B中固体溶解,产生无色气体,C试管中产生白色沉淀,实验的目的是比较碳酸、醋酸、硅酸的酸性强弱,
故答案为:石灰石;C试管中产生白色沉淀.
点评:本题考查了实验方案设计,题目难度中的,注意根据气体的性质及密度选择相应的收集方法以及实验设计的方案的设计,侧重于考查学生对实验原理的把握和对仪器的使用.

练习册系列答案
相关题目
常温下下列有关CH3COONa溶液中的关系式不正确的是( )
| A、C((H +)>1.0×10-7mol/L |
| B、C(CH3COOˉ)+C(OHˉ)=C(Na +)+C(H +) |
| C、C(CH3COOˉ)+C(CH3COOH)=C(Na +) |
| D、C(OHˉ)=C(CH3COOH)+C(H +) |
下列物质中,含有共价键的离子化合物是( )
| A、NaCl |
| B、H2O |
| C、CaCl2 |
| D、KOH |
 (1)图中所示反应是
(1)图中所示反应是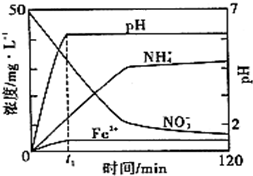 I.铁盐、亚铁盐是实验室常用的药品.
I.铁盐、亚铁盐是实验室常用的药品.