题目内容
为探索工业废料的再利用,某化学兴趣小组设计了如图实验方案,用含有铝、铁和铜的合金制取氯化铝、绿矾晶体(FeSO4?7H2O)和胆矾晶体.

请回答:
(1)步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 ,该操作中除用到烧杯和玻璃棒外,还必须用到的玻璃仪器有 .
(2)溶液A中的离子主要有 ;试剂X是 .
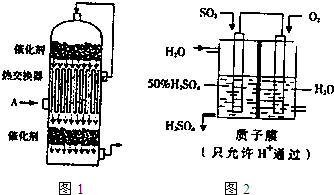
(3)进行步骤Ⅱ时,该小组用如上右图所示装置及试剂将制得的CO2气体通入溶液A中.一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是(用离子方程式表示) ;为了避免固体C减少,改进的措施是 .
(4)用固体F制备CuSO4溶液的化学方程式是2Cu+O2+2H2SO4=2CuSO4+2H2O,这样做的好处是 .

请回答:
(1)步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是
(2)溶液A中的离子主要有
(3)进行步骤Ⅱ时,该小组用如上右图所示装置及试剂将制得的CO2气体通入溶液A中.一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是(用离子方程式表示)
(4)用固体F制备CuSO4溶液的化学方程式是2Cu+O2+2H2SO4=2CuSO4+2H2O,这样做的好处是
考点:制备实验方案的设计,物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:铝、铁和铜的合金中只有金属铝可以和氢氧化钠之间反应生成溶液A偏铝酸钠,固体B是金属铁和金属铜,A中通入过量的二氧化碳可以得到氢氧化铝沉淀C和碳酸氢钠溶液D,金属铁可以和硫酸之间发生反应生成硫酸亚铁和氢气,但是金属铜和稀硫酸之间不反应,硫酸亚铁溶液蒸发浓缩、冷却结晶可以获得绿矾晶体,金属铜可以获得胆矾晶体.
(1)固体和液体的分离用过滤法,过滤用到的仪器:烧杯、玻璃棒、漏斗等;
(2)根据步骤Ⅰ加过量的氢氧化钠发生的反应以及金属铁、铜的性质区别进行解答;
(3)制得的CO2气体中混有氯化氢气体,用饱和的碳酸氢钠除去;
(4)根据铜、稀硫酸的性质来判断反应的发生,并结合产物一会原子的利用率来回答其优点.
(1)固体和液体的分离用过滤法,过滤用到的仪器:烧杯、玻璃棒、漏斗等;
(2)根据步骤Ⅰ加过量的氢氧化钠发生的反应以及金属铁、铜的性质区别进行解答;
(3)制得的CO2气体中混有氯化氢气体,用饱和的碳酸氢钠除去;
(4)根据铜、稀硫酸的性质来判断反应的发生,并结合产物一会原子的利用率来回答其优点.
解答:
解:铝、铁和铜的合金中只有金属铝可以和氢氧化钠之间反应生成溶液A偏铝酸钠,固体B是金属铁和金属铜,A中通入过量的二氧化碳可以得到氢氧化铝沉淀C和碳酸氢钠溶液D,金属铁可以和硫酸之间发生反应生成硫酸亚铁和氢气,但是金属铜和稀硫酸之间不反应,硫酸亚铁溶液蒸发浓缩、冷却结晶可以获得绿矾晶体,金属铜可以获得胆矾晶体.
(1)步骤Ⅰ加过量的氢氧化钠,金属铝和氢氧化钠反应,金属铝溶解其中生成偏铝酸钠溶液,金属铁和金属铜不与氢氧化钠反应,将它们分离用过滤;步骤Ⅰ过滤得到的滤液成分为偏铝酸钠,步骤Ⅱ中向偏铝酸钠中通入足量的二氧化碳,会得到纯净的氢氧化铝沉淀,溶液中的溶质为碳酸氢钠,将它们分离用过滤;步骤Ⅲ中金属铁和金属铜不与氢氧化钠反应,铁和硫酸反应而金属铜不反应将它们分离用过滤,过滤用到的玻璃仪器:烧杯、玻璃棒、漏斗等.
故答案为:过滤;漏斗;
(2)步骤Ⅰ加过量的氢氧化钠,因铝与碱反应生成偏铝酸钠和氢气,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,金属铁和金属铜不与氢氧化钠反应,所以溶液A中的离子主要有AlO2-、Na+、OH-;本实验的目的是用含有铝、铁和铜的合金制取氯化铝、绿矾晶体(FeSO4?7H2O)和胆矾晶体,金属铁和金属铜不与氢氧化钠反应,铁和硫酸反应生成硫酸亚铁而金属铜不反应,可以实现三种金属的分离,所以试剂X是稀硫酸,
故答案为:AlO2-、Na+、OH-;稀硫酸;
(3)进行步骤Ⅱ时,该小组用如图2所示装置及试剂将制得的CO2气体通入溶液A中.一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是二氧化碳气体中含有从盐酸中挥发出的氯化氢气体,氯化氢在水中溶解了部分沉淀氢氧化铝,发生的反应为Al(OH)3+3H+=Al3++3H2O,为了避免固体C减少,可在制取二氧化碳的收集装置中增加一个洗去氯化氢的装置,二氧化碳在饱和碳酸氢钠中不溶,氯化氢和碳酸氢钠反应生成二氧化碳气体,所以可在装置I和Ⅱ之间增加一个盛有饱和碳酸氢钠溶液的洗气瓶,除去二氧化碳中的氯化氢,
故答案为:Al(OH)3+3H+=Al3++3H2O;在装置I和Ⅱ之间增加一个盛有饱和碳酸氢钠溶液的洗气瓶;
(4)铜不能和稀硫酸反应,但是当加热并通入空气之后,铜和氧气反应生成氧化铜,然后氧化铜会和硫酸反应生成硫酸铜,即2Cu+O2+2H2SO4=2CuSO4+2H2O,不会产生污染大气的气体,故答案为:节约原料,防止环境污染.
(1)步骤Ⅰ加过量的氢氧化钠,金属铝和氢氧化钠反应,金属铝溶解其中生成偏铝酸钠溶液,金属铁和金属铜不与氢氧化钠反应,将它们分离用过滤;步骤Ⅰ过滤得到的滤液成分为偏铝酸钠,步骤Ⅱ中向偏铝酸钠中通入足量的二氧化碳,会得到纯净的氢氧化铝沉淀,溶液中的溶质为碳酸氢钠,将它们分离用过滤;步骤Ⅲ中金属铁和金属铜不与氢氧化钠反应,铁和硫酸反应而金属铜不反应将它们分离用过滤,过滤用到的玻璃仪器:烧杯、玻璃棒、漏斗等.
故答案为:过滤;漏斗;
(2)步骤Ⅰ加过量的氢氧化钠,因铝与碱反应生成偏铝酸钠和氢气,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,金属铁和金属铜不与氢氧化钠反应,所以溶液A中的离子主要有AlO2-、Na+、OH-;本实验的目的是用含有铝、铁和铜的合金制取氯化铝、绿矾晶体(FeSO4?7H2O)和胆矾晶体,金属铁和金属铜不与氢氧化钠反应,铁和硫酸反应生成硫酸亚铁而金属铜不反应,可以实现三种金属的分离,所以试剂X是稀硫酸,
故答案为:AlO2-、Na+、OH-;稀硫酸;
(3)进行步骤Ⅱ时,该小组用如图2所示装置及试剂将制得的CO2气体通入溶液A中.一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是二氧化碳气体中含有从盐酸中挥发出的氯化氢气体,氯化氢在水中溶解了部分沉淀氢氧化铝,发生的反应为Al(OH)3+3H+=Al3++3H2O,为了避免固体C减少,可在制取二氧化碳的收集装置中增加一个洗去氯化氢的装置,二氧化碳在饱和碳酸氢钠中不溶,氯化氢和碳酸氢钠反应生成二氧化碳气体,所以可在装置I和Ⅱ之间增加一个盛有饱和碳酸氢钠溶液的洗气瓶,除去二氧化碳中的氯化氢,
故答案为:Al(OH)3+3H+=Al3++3H2O;在装置I和Ⅱ之间增加一个盛有饱和碳酸氢钠溶液的洗气瓶;
(4)铜不能和稀硫酸反应,但是当加热并通入空气之后,铜和氧气反应生成氧化铜,然后氧化铜会和硫酸反应生成硫酸铜,即2Cu+O2+2H2SO4=2CuSO4+2H2O,不会产生污染大气的气体,故答案为:节约原料,防止环境污染.
点评:本题是对物质的分离和提纯知识点的考查,注意掌握铝、铁和铜及其化合物的性质是解答本题的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验操作或装置正确的是( )
A、 |
B、 |
C、 |
D、 |
与乙炔具有相同的碳、氢百分含量,但既不是同系物又不是同分异构体的是( )
| A、甲烷 | B、苯 | C、乙烯 | D、乙烷 |

 E.
E. 请选择正确答案的字母填在相应的空格里.
请选择正确答案的字母填在相应的空格里.