题目内容
浓度为0.1mol/L的三种酸:盐酸、硫酸、磷酸,当它们的体积均为10mL时,溶液中H+的浓度由大到小的顺序是 .
考点:电解质在水溶液中的电离
专题:电离平衡与溶液的pH专题
分析:相同温度下的同浓度、同体积的不同酸溶液,氢离子个数越多、电离越完全的酸中氢离子浓度越大.
解答:
解:浓度均为 0.1mol?L-1的盐酸、硫酸和磷酸四种稀溶液,盐酸的一元强酸,完全电离,硫酸是二元强酸,磷酸是三元中强酸,电离程度很小,所以溶液中氢离子浓度大小顺序是:硫酸>盐酸>磷酸.
故答案为:硫酸>盐酸>磷酸.
故答案为:硫酸>盐酸>磷酸.
点评:本题考查学生电解质的电离知识,注意知识的迁移和应用是关键,难度中等.

练习册系列答案
相关题目
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,分别与等量AgNO3溶液反应完全,则消耗三种溶液的体积比为( )
| A、1:2:3 |
| B、1:1:1 |
| C、6:3:2 |
| D、3:2:1 |
下列物质均可用作燃料,其中最环保的是( )
| A、甲醇 | B、天然气 |
| C、液化石油气 | D、氢气 |
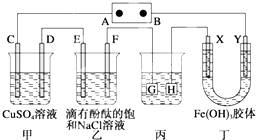 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答:
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.请回答: