题目内容
下列说法正确的是( )
①1molCH3+离子中所含电子数为8NA
②56g铁原子和标况下22.4LCl2反应时共失去电子数为2NA
③在标准状况下,1mol H2和1mol H2O所占的体积都约是22.4L
④在标准状况下,22.4L由N2和N2O组成的混合气体中,所含有的氮原子的物质的量2mol.
①1molCH3+离子中所含电子数为8NA
②56g铁原子和标况下22.4LCl2反应时共失去电子数为2NA
③在标准状况下,1mol H2和1mol H2O所占的体积都约是22.4L
④在标准状况下,22.4L由N2和N2O组成的混合气体中,所含有的氮原子的物质的量2mol.
| A、只有②③④ | B、只有①②④ |
| C、只有②④ | D、只有④ |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:①根据CH3+离子是阳离子来分析;
②根据n=
和n=
分别求出铁和氯气的物质的量,然后根据反应的情况来分析;
③标况下,水为液态;
④根据n=
求出混合气体的物质的量,然后根据N2和N2O均有2个N原子来分析.
②根据n=
| m |
| M |
| V |
| Vm |
③标况下,水为液态;
④根据n=
| V |
| Vm |
解答:
解:①CH3+离子是阳离子,故1molCH3+离子中含8mol电子,即电子数为8NA,故①正确;
②根据n=
可知铁的物质的量n=
=1mol,1mol铁与氯气反应时需要1.5mol氯气;而氯气的物质的量n=
=
=1mol,故氯气不足,反应转移电子数由氯气决定.1molCl2与铁反应后变为-1价,故1molCl2转移2mol电子,个数为2NA个,故②正确;
③标况下,水为液态,故③错误;
④根据n=
可知混合气体的物质的量n=
=1mol,由于N2和N2O均有2个N原子,故1mol混合气体中含2mol氮原子,故④正确.
故选B.
②根据n=
| m |
| M |
| 56g |
| 56g/mol |
| V |
| Vm |
| 22.4L |
| 22.4L/mol |
③标况下,水为液态,故③错误;
④根据n=
| V |
| Vm |
| 22.4L |
| 22.4L/mol |
故选B.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的使用和物质的结构是关键,难度不大.

练习册系列答案
相关题目
下列化学用语表示不正确的是( )
A、甲基的电子式: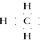 |
B、氮原子的电子排布图: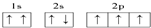 |
| C、氯离子的最外层电子排布:3s23p6 |
D、硫离子的结构示意图: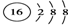 |
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L的戊烷所含的分子数为0.5NA |
| B、28g乙烯所含共用电子对数目为4NA |
| C、1mol苯中含有碳碳双键的数目为3NA |
| D、2.8g聚乙烯中含有的碳原子数为0.2NA |
下列各组描述正确的是( )
| A、化工生产要遵守三原则:充分利用原料、充分利用能量、保护环境. ①燃烧时使用沸腾炉 ②制盐酸时将氯气在氢气中燃烧 ③制硫酸时使用热交换器 这3种化工生产分别符合以上某原则 |
| B、①用燃烧的方法鉴别甲烷、乙烯和乙炔 ②用酒精萃取溴水中的溴 ③用水鉴别硝酸铵和氢氧化钠固体 ④用互滴法鉴别Na2CO3、盐酸、BaCl2、NaCl四种溶液 以上均能达到实验目的 |
| C、①用硫粉覆盖地下撒有的汞 ②金属钠着火用泡沫灭火器或干粉灭火器扑灭 ③用热碱溶液洗去试管内壁的硫 ④用湿的红色石蕊试纸检验氨气是否集满 以上操作均合理 |
| D、①过氧化氢:火箭燃料 ②碳酸氢钠:食品发酵剂 ③钠:制氢氧化钠 ④硫酸:制蓄电池 以上物质的用途均合理 |
下列关于环境问题的说法不正确的是( )
| A、在燃煤中加入CaO可以减少SO2的排放 |
| B、“白色污染”的发生说明有些合成材料的废弃物会造成严重的环境问题 |
| C、pH在5.6-7.0之间的降水通常称为酸雨 |
| D、废旧电池渗出的重金属离子会造成地下水和土壤的污染 |
 向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题:
向Ba(OH)2溶液中逐滴加入稀硫酸.请完成下列问题: