题目内容
16.下列说法正确的是( )| A. | 同一物质的固、液、气三种状态的熵值相同 | |
| B. | NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g);△H=+185.57 kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 | |
| C. | 焓变或熵变均可以单独作为反应自发性的判据 | |
| D. | 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 |
分析 A.混乱度越大,熵值越大;
B.由反应可知,△H>0、△S>0,能自发进行,可知△H-T△S<0;
C.利用综合判据△H-T△S与0的关系;
D.使用催化剂,只能改变反应速率,与反应的方向无关.
解答 解:A.混乱度越大,熵值越大,则同一物质的固、液、气三种状态的熵值由s→g增大,故A错误;
B.由反应可知,△H>0、△S>0,能自发进行,可知△H-T△S<0,可知体系有自发地向混乱度增加的方向转变的倾向,故B正确;
C.利用综合判据△H-T△S与0的关系,△H-T△S<0能自发进行,不能单独使用焓变、熵变判断反应进行的方向,故C错误;
D.使用催化剂,只能改变反应速率,与反应的方向无关,不能改变化学反应进行的方向,故D错误;
故选B.
点评 本题考查反应热与焓变,为高频考点,把握焓变、熵变的判断及反应进行方向的综合判据为解答的关键,侧重分析与应用能力的考查,注意不能单独使用焓变、熵变判断反应进行的方向,题目难度不大.

练习册系列答案
相关题目
6.在饱和Mg(OH)2溶液中,c(OH-)=1.0×10-4 mol•L-1.若往该溶液中加入NaOH溶液,使溶液的c(OH-)变为原来的10倍,则Mg(OH)2的溶解度在理论上将( )
| A. | 变为原来的10-3倍 | B. | 变为 原来的10-2倍 | ||
| C. | 变为原来的103倍 | D. | 不发生变化 |
7.下列关于1S电子在原子核外出现的概率分布图(电子云)的说法中,正确的是( )


| A. | 通常用小黑点来表示电子的多少 | |
| B. | 小黑点密表示在该核外空间的电子数多 | |
| C. | 小黑点密表示在该核外空间的单位体积内电子出现的概率大 | |
| D. | 通常用小黑点来表示电子绕核作高速圆周运动 |
4.下列对于废弃塑料制品的处理方法中,最为恰当的是( )
| A. | 将废弃物切成碎片,混在垃圾中填埋于土壤中 | |
| B. | 将废弃物焚烧 | |
| C. | 将废弃物加工成防水涂料或汽油,以节约资源 | |
| D. | 将废弃物倾倒在海洋中 |
11.已知:2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-452kJ•mol-1
根据以上热化学方程式判断,下列说法正确的是( )
2Na2O2(s)+2CO2(g)=2Na2CO3(s)+O2(g)△H=-452kJ•mol-1
根据以上热化学方程式判断,下列说法正确的是( )
| A. | 1molCO 完全燃烧,放出热量为 283 J | |
| B. | Na2O2(s)+CO2(s)=Na2CO3(s)+$\frac{1}{2}$ O2(g)△H=-226 kJ•mol-1 | |
| C. | CO(g)与 Na2O2(s)反应放出 509 kJ 热量时,电子转移数为 1.204×1024 | |
| D. | CO 的燃烧热为 566 kJ•mol-1 |
1.已知:还原性强弱:I->Fe2+.往100mL碘化亚铁溶液中缓慢通入3.36L(标准状况)氯气,反应完成后溶液中有一半的Fe2+被氧化成Fe3+.则原碘化亚铁溶液的物质的量浓度为( )
| A. | 0.12 mol•L-1 | B. | 0.1 mol•L-1 | C. | 1.2 mol•L-1 | D. | 1.0 mol•L-1 |
8.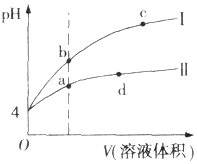 常温下,pH均为4的HCl和CH3COOH溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断正确的是( )
常温下,pH均为4的HCl和CH3COOH溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断正确的是( )
 常温下,pH均为4的HCl和CH3COOH溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断正确的是( )
常温下,pH均为4的HCl和CH3COOH溶液分别加水稀释,pH随溶液体积变化的曲线如图所示.据图判断正确的是( )| A. | pH=4的HCl溶液中H2O电离出的c(H+)=10-4 mol.L-1 | |
| B. | 曲线I为CH3COOH溶液的稀释曲线 | |
| C. | a、d点溶液和NaOH溶液完全反应时消耗的NaOH的物质的量相等 | |
| D. | a、b、c三点溶液中Kw:c=b<a |
5.下列说法不正确的是( )
| A. | 油脂是高级脂肪酸和甘油生成的酯 | |
| B. | 米饭在嘴中越咀嚼越甜的原因是淀粉水解生成甜味物质 | |
| C. | 油脂、乙醇是人体必需的营养物质 | |
| D. | 水果因含有酯类物质而具有香味 |
7.莫尔法是一种沉淀滴定法,以K2CrO4为指示剂,用标准硝酸银溶液滴定待测液,进行测定溶液中Cl-的浓度.已知:
滴定终点的现象是滴入最后一滴标准液时,生成砖红色沉淀,且30s内不褪色.终点现象对应的离子反应方程式为2Ag++CrO42-=Ag2CrO4↓.为了测定产品中(NH4)2Cr2O7的含量,称取样品0.150 0g,置于锥形瓶中,加50mL水,再加入2g KI(过量)及稍过量的稀硫酸溶液,摇匀,暗处放置10min,然后加150mL蒸馏水并加入3mL 0.5%淀粉溶液,用0.1000mol/L Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液30.00mL,则上述产品中(NH4)2Cr2O7的纯度为84%. (假定杂质不参加反应,已知:①Cr2O${\;}_{7}^{2-}$+6I-+14H+═2Cr3++3I2+7H2O,I2+2S2O${\;}_{3}^{2-}$═2I-+S4O${\;}_{6}^{2-}$;②(NH4)2Cr2O7的摩尔质量为252g/moL).
| 银盐 性质 | AgCl | AgBr | Ag2CrO4 |
| 颜色 | 白 | 浅黄 | 砖红 |