题目内容
已知几种难溶电解质的溶度积如下表所示:
(1)AgBr、AgI、FeS、ZnS、CuS的溶解能力由大到小的顺序 为: .
(2)向饱和的AgI溶液中加入固体硝酸银,则硝酸银 (填“增大”、“减小”或“不变”),若改加AgBr固体,则AgI (填“增大”、“减小”或“不变”).
(3)在25℃时,向100mL浓度均为0.1mol?L-1FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是 (用沉淀物的化学式表示).
(4)在25℃时,把ZnS加入蒸馏水中,一定时间后达到如下平衡:ZnS(s)═Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是
A.加入少量CuS固体B.加入少量FeS固体C.加入少量FeCl2固体D.加入少量CuCl2固体.
| 几种难溶电解质的Ksp(25℃) | |
| 沉淀溶解平衡 | Ksp |
AgBr(s) Ag+(aq)+Br-(aq) | 5,0×10-13mol2?L-2 |
AgI(s) Ag+(aq)+I-(aq) | 8.3×10-17mol2?L-2 |
FeS(s) Fe2+(aq)+S2-(aq) | 6.3×10-18mol2?L-2 |
ZnS(s) Zn2+(aq)+S2-(aq) | 1.6×10-24mol2?L-2 |
CuS(s) Cu2+(aq)+S2-(aq) | 1.3×10-36mol2?L-2 |
(2)向饱和的AgI溶液中加入固体硝酸银,则硝酸银
(3)在25℃时,向100mL浓度均为0.1mol?L-1FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是
(4)在25℃时,把ZnS加入蒸馏水中,一定时间后达到如下平衡:ZnS(s)═Zn2+(aq)+S2-(aq),下列措施可使ZnS减少的是
A.加入少量CuS固体B.加入少量FeS固体C.加入少量FeCl2固体D.加入少量CuCl2固体.
考点:难溶电解质的溶解平衡及沉淀转化的本质
专题:电离平衡与溶液的pH专题
分析:(1)化学式相似的物质的溶度积常数越小,则物质越难溶;
(2)在一定温度下,向AgI的饱和溶液中存在沉淀溶解平衡,平衡状态下存在溶度积常数,依据平衡影响因素分析平衡的变化;
(3)难溶电解质的溶度积越小,加入Na2S溶液时越易生成沉淀;
(4)使ZnS减少,应使平衡ZnS(s)?Zn2+(aq)+S2-(aq)向正向移动,从难溶电解质的转化的角度解答.
(2)在一定温度下,向AgI的饱和溶液中存在沉淀溶解平衡,平衡状态下存在溶度积常数,依据平衡影响因素分析平衡的变化;
(3)难溶电解质的溶度积越小,加入Na2S溶液时越易生成沉淀;
(4)使ZnS减少,应使平衡ZnS(s)?Zn2+(aq)+S2-(aq)向正向移动,从难溶电解质的转化的角度解答.
解答:
解:(1)根据化学式相似的物质的溶度积常数越小,物质越难溶,可知常温下在水中溶解能力AgBr>AgI>FeS>ZnS>CuS,
故答案为:AgBr>AgI>FeS>ZnS>CuS;
(2)加入AgNO3固体,会增加银离子浓度,沉淀溶解平衡AgI(s)?Ag+(aq)+I-(aq),左移,AgNO3固体减小,加入固体AgBr,AgBr的溶解性大于AgI,所以平衡状态下AgBr溶液中的银离子浓度大于AgI溶液中的银离子浓度,所以碘化银沉淀溶解平衡左移,碘化银沉淀增大,
故答案为:减小;增大;
(3)难溶电解质的溶度积越小,加入Na2S溶液时越易生成沉淀,所以在25℃时,向100mL浓度均为0.1mol?L-1FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是CuS、ZnS、FeS,
故答案为:CuS、ZnS、FeS;
(4)加入少量CuS固体、FeS固体,二者都难溶于水,而加入少量FeCl2固体或CuCl2固体,可满足c(Fe2+)×c(S2-)或c(Cu2+)×c(S2-)大于Ksp,可生成CuS或FeS沉淀,进而促进ZnS的溶解,
故选CD.
故答案为:AgBr>AgI>FeS>ZnS>CuS;
(2)加入AgNO3固体,会增加银离子浓度,沉淀溶解平衡AgI(s)?Ag+(aq)+I-(aq),左移,AgNO3固体减小,加入固体AgBr,AgBr的溶解性大于AgI,所以平衡状态下AgBr溶液中的银离子浓度大于AgI溶液中的银离子浓度,所以碘化银沉淀溶解平衡左移,碘化银沉淀增大,
故答案为:减小;增大;
(3)难溶电解质的溶度积越小,加入Na2S溶液时越易生成沉淀,所以在25℃时,向100mL浓度均为0.1mol?L-1FeCl2、ZnCl2、CuCl2的混合溶液中逐滴加入Na2S溶液,生成的沉淀的先后顺序是CuS、ZnS、FeS,
故答案为:CuS、ZnS、FeS;
(4)加入少量CuS固体、FeS固体,二者都难溶于水,而加入少量FeCl2固体或CuCl2固体,可满足c(Fe2+)×c(S2-)或c(Cu2+)×c(S2-)大于Ksp,可生成CuS或FeS沉淀,进而促进ZnS的溶解,
故选CD.
点评:本题考查了沉淀溶解平衡的分析判断和应用,为高频考点,侧重于学生的分析能力的考查,注意把握影响平衡移动的因素,主要是分析沉淀溶解平衡的影响因素的分析判断平衡移动的方向,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
A、B、C、D、E是原子序数依次增大的五种短周期元素.B和D同主族,可组成共价化合物DB2,B和C最外层电子数之和与E的最外层电子数相同,25℃时0.01mol?L-1A和E形成化合物的水溶液pH为2.下列说法正确的是( )
| A、由于非金属性B>D,则A、B组成化合物的沸点高于A、D组成的化合物 |
| B、在C、B形成的两种离子化合物中阴阳离子的个数比分别为1:2和1:1 |
| C、原子半径由大到小排列的是:C>D>E>B>A |
| D、B、C、E三种元素组成化合物的水溶液一定显碱性 |
将一小块金属钠投入到CuSO4溶液中,不可能得到的产物是( )
| A、Cu |
| B、H2 |
| C、Cu(OH)2 |
| D、Na2SO4 |
下列离子方程式正确的是:
| A、氢氧化铁中加入氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| B、铝粉溶于氢氧化钠溶液中:Al+2OH-=AlO2-+H2↑ |
| C、在酸性的硫酸亚铁溶液中加入双氧水:2Fe2++H2O2+2H+=2Fe3++2H2O |
| D、硫化氢气体通入氯化铁溶液中:Fe3++H2S=Fe2++S↓+2H+ |
已知反应mx(g)+ny(g)?qZ(g)的△H<0,m+n>q,在恒容密闭容器中反应达到平衡时,下列说法正确的是( )
| A、通入稀有气体使压强增大,平衡向正反应方向移动 |
| B、x的正反应速率是y的逆反应速率的n/m倍 |
| C、降低温度,混合气体的平均相对分子质量变大 |
| D、增加X的物质的量,y的转化率降低 |
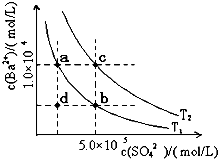 回答下列问题:
回答下列问题: