题目内容
以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等.实验室模拟工业以硫酸渣制备铁红(Fe2O3),过程如下:

(1)硫酸渣的成分中属于两性氧化物的是 ,写出酸溶过程硫酸渣与稀硫酸反应的离子反应方程式(任意两个): 、
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是 (部分阳离子以氢氧化物形式沉淀时溶液的pH见下表)
(3)滤渣A的主要成分为 ,滤液B可以回收的物质有Na2SO4、MgSO4和
(4)第二次过滤得到的沉淀加水进行洗涤,如何证明沉淀一定洗涤干净?请简单描述一下实验操作: .

(1)硫酸渣的成分中属于两性氧化物的是
(2)生产过程中,为了确保铁红的纯度,氧化过程需要调节溶液的pH的范围是
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 |
(4)第二次过滤得到的沉淀加水进行洗涤,如何证明沉淀一定洗涤干净?请简单描述一下实验操作:
考点:铁的氧化物和氢氧化物,难溶电解质的溶解平衡及沉淀转化的本质,镁、铝的重要化合物
专题:几种重要的金属及其化合物
分析:硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,稀硫酸溶解主要除去不与酸反应的SiO2,再加氢氧化钠调节PH值3.2~3.8主要是使三价铁沉淀,而二价镁,三价铝都不沉淀而被除去,最后洗涤、烘干、研磨使氢氧化铁分解生成氧化铁,从而得到实验目的;
(1)氧化铝是两性氧化物,可以和硫酸反应生成硫酸铝和水;氧化铁是碱性氧化物,可以和硫酸反应生成硫酸铁和水;
(2)根据几种离子沉淀的pH,应选择使Fe3+沉淀完全而其他离子不沉淀;
(3)二氧化硅不和酸反应;因加入的是氢氧化钠来调节PH,所以滤液B中应是未沉淀离子的硫酸盐和硫酸钠;
(4)洗涤干净的实验操作为取最后一次洗涤液,加入BaCl2溶液,不产生白色沉淀,则证明沉淀洗涤干净.
(1)氧化铝是两性氧化物,可以和硫酸反应生成硫酸铝和水;氧化铁是碱性氧化物,可以和硫酸反应生成硫酸铁和水;
(2)根据几种离子沉淀的pH,应选择使Fe3+沉淀完全而其他离子不沉淀;
(3)二氧化硅不和酸反应;因加入的是氢氧化钠来调节PH,所以滤液B中应是未沉淀离子的硫酸盐和硫酸钠;
(4)洗涤干净的实验操作为取最后一次洗涤液,加入BaCl2溶液,不产生白色沉淀,则证明沉淀洗涤干净.
解答:
解:硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,稀硫酸溶解主要除去不与酸反应的SiO2,再加氢氧化钠调节PH值3.2~3.8主要是使三价铁沉淀,而二价镁,三价铝都不沉淀而被除去,最后洗涤、烘干、研磨使氢氧化铁分解生成氧化铁,从而得到实验目的;
(1)氧化铝是两性氧化物,可以和硫酸反应生成硫酸铝和水,离子方程式为:Al2O3+6H+=2Al3++3H2O;
氧化铁是碱性氧化物,可以和硫酸反应生成硫酸铁和水,离子方程式为Fe2O3+6H+═2Fe3++3H2O,
故答案为:Al2O3;Al2O3+6H+=2Al3++3H2O;Fe2O3+6H+=2Fe3++3H2O;
(2)根据几种离子沉淀的pH,使Fe3+沉淀完全的PH为3.2,其他离子开始沉淀PH为3.8,因此所选PH因介于3.2和3.8之间,
故答案为:3.2~3.8;
(3)因二氧化硅不与硫酸反应,故“滤渣A”主要成份为SiO2;未沉淀的离子为Na+、Mg2+、Al3+,故滤液B可以回收的物质有Na2SO4、Al2(SO4)3、MgSO4,
故答案为:SiO2;Al2(SO4)3;
(4)洗涤干净的实验操作为取最后一次洗涤液,加入BaCl2溶液,不产生白色沉淀,则证明沉淀洗涤干净,
故答案为:取最后一次洗涤液,加入BaCl2溶液,不产生白色沉淀,则证明沉淀洗涤干净.
(1)氧化铝是两性氧化物,可以和硫酸反应生成硫酸铝和水,离子方程式为:Al2O3+6H+=2Al3++3H2O;
氧化铁是碱性氧化物,可以和硫酸反应生成硫酸铁和水,离子方程式为Fe2O3+6H+═2Fe3++3H2O,
故答案为:Al2O3;Al2O3+6H+=2Al3++3H2O;Fe2O3+6H+=2Fe3++3H2O;
(2)根据几种离子沉淀的pH,使Fe3+沉淀完全的PH为3.2,其他离子开始沉淀PH为3.8,因此所选PH因介于3.2和3.8之间,
故答案为:3.2~3.8;
(3)因二氧化硅不与硫酸反应,故“滤渣A”主要成份为SiO2;未沉淀的离子为Na+、Mg2+、Al3+,故滤液B可以回收的物质有Na2SO4、Al2(SO4)3、MgSO4,
故答案为:SiO2;Al2(SO4)3;
(4)洗涤干净的实验操作为取最后一次洗涤液,加入BaCl2溶液,不产生白色沉淀,则证明沉淀洗涤干净,
故答案为:取最后一次洗涤液,加入BaCl2溶液,不产生白色沉淀,则证明沉淀洗涤干净.
点评:本题考查实验的探究与评价,难度中等.涉及物质的性质、离子方程式的书写等方面的知识,侧重学生分析、解决问题能力的培养.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
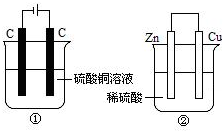 如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200mL,开始工作前电解质溶液的浓度均为0.5mol/L,工作一段时间后,测得有0.02mol电子通过,若忽略溶液体积的变化,下列叙述正确的是( )| A、产生气体体积 ①=② |
| B、①中阴极质量增加,②中正极质量减小 |
| C、溶液的pH变化:①减小,②增大 |
| D、电极反应式:①中阳极:4OH--4e-=2H2O+O2↑②中负极:2H++2e-=H2↑ |
 2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系.已知充电时电池总反应为:LiMn2O4═Li1-xMn2O4+xLi,下列叙述正确的是( )
2013年3月我国科学家报道了如图所示的水溶液锂离子电池体系.已知充电时电池总反应为:LiMn2O4═Li1-xMn2O4+xLi,下列叙述正确的是( )| A、放电时,正极反应为xLi++xe-═xLi |
| B、放电时,a极锂的化合价不发生变化 |
| C、充电时,b极发生氧化反应 |
| D、充电时,溶液中的Li+从b极向a极迁移 |
下列说法正确的是( )
| A、能通过化合反应制得FeCl2和Fe(OH)3 |
| B、7.8gNa2O2与CO2完全反应,转移0.2mol电子 |
| C、Na、Fe分别与不足量的稀硫酸反应所得溶液均呈中性 |
| D、NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
下列说法错误的是( )
| A、电解饱和食盐水可制取烧碱、氯气、氢气 |
| B、从海水中可提取镁、溴、碘等物质 |
| C、粗铜(含少量Zn、Fe、Pt等)电解精炼后,溶液中金属阳离子只有Fe2+、Zn2+ |
| D、在镀件上镀铜,镀件作阴极 |
下列有关实验的做法正确的是( )
| A、用pH试纸测氯水的pH |
| B、用托盘天平称取5.72 g NaCl晶体 |
| C、用酸式滴定管量取20.00 mL的酸性KMnO4溶液 |
| D、用带磨口玻璃塞的试剂瓶保存Na2CO3溶液 |

 (1)25.C时,0.1mol/L的HA溶液中
(1)25.C时,0.1mol/L的HA溶液中