题目内容
1.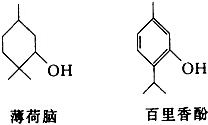 下列物质是几种常见香精的主要成分:
下列物质是几种常见香精的主要成分:回答下列问题:
(1)薄荷脑的分子式为C9H18O.
(2)鉴别薄荷脑和百里香酚,可选用的试剂是溴水(或氯化铁溶液).
(3)写出百里香酚与足量浓溴水反应的化学方程式:
 .
.(4)写出往百里香酚钠溶液中通入CO2发生反应的化学方程式:
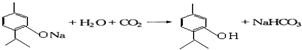 .
.
分析 (1)由结构简式可知分子式;
(2)百里香酚含酚-OH,结合酚的性质分析;
(3)百里香酚与足量浓溴水发生取代反应生成沉淀;
(4)百里香酚钠溶液中通入CO2气体,发生强酸制取弱酸的反应,生成酚和碳酸氢钠.
解答 解:(1)由结构简式可知分子式为C9H18O,故答案为:C9H18O;
(2)百里香酚含酚-OH,与溴水发生取代反应生成沉淀,与氯化铁发生显色反应,而薄荷脑不能,则鉴别试剂为溴水(或氯化铁溶液),故答案为:溴水(或氯化铁溶液);
(3)百里香酚与足量浓溴水反应的化学方程式为 ,故答案为:
,故答案为: ;
;
(4)往百里香酚钠溶液中通入CO2气体的化学反应方程式为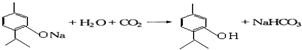 ,
,
故答案为: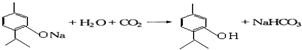 .
.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查酚、醇的性质,利用官能团的差异性进行鉴别,注意酚和溴发生取代反应位置,题目难度不大.

练习册系列答案
 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案
相关题目
11.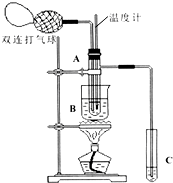 乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:
请回答下列问题:
(1)试管A内,60℃~80℃时发生的主要反应的化学方程式为2CH3CHO+O2$→_{CuO}^{60℃-80℃}$2CH3COOH;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在试管A的反应液中;目的是测量反应溶液的温度;当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处,目的是收集含乙酸的馏分;
(3)烧杯B的作用是使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C;烧杯B内盛装的液体可以是乙二醇或甘油(在题给物质中确定).
 乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:
乙醛在氧化铜催化剂存在的条件下,可以被空气氧化成乙酸.依据此原理设计实验制得并在试管C中收集到少量乙酸溶液(如图所示:试管A中装有40%的乙醛水溶液、氧化铜粉末;试管C中装有适量蒸馏水;烧杯B中装有某液体).已知在60℃~80℃时用双连打气球鼓入空气即可发生乙醛的氧化反应,连续鼓入十几次反应基本完全.有关物质的沸点见表:| 物质 | 乙醛 | 乙酸 | 甘油 | 乙二醇 | 水 |
| 沸点 | 20.8℃ | 117.9℃ | 290℃ | 197.2℃ | 100℃ |
(1)试管A内,60℃~80℃时发生的主要反应的化学方程式为2CH3CHO+O2$→_{CuO}^{60℃-80℃}$2CH3COOH;
(2)如图所示在实验的不同阶段,需要调整温度计在试管A内的位置,在实验开始时温度计水银球的位置应在试管A的反应液中;目的是测量反应溶液的温度;当试管A内的主要反应完成后温度计水银球的位置应在试管A的支管口处,目的是收集含乙酸的馏分;
(3)烧杯B的作用是使试管A内的反应液均匀受热发生反应,使生成的乙酸变成蒸气进入试管C;烧杯B内盛装的液体可以是乙二醇或甘油(在题给物质中确定).
12.下列组合中不可能形成喷泉的是( )
| A. | HCl和H2O | B. | O2和H2O | C. | NH3和H2O | D. | CO2和NaOH溶液 |
9.5.3g某一元醛与过量新制Cu(OH)2的碱性浊液加热充分反应,生成的红色沉淀经过滤、洗涤、烘干称其质量为7.2g,则该醛为( )
| A. | HCHO | B. | CH3CHO | C. | C5H17CHO | D. | C6H5CHO |
16.反应2NO+O2=2NO2,不能使该反应的反应速率增大的是( )
| A. | 及时分离出NO2气体 | B. | 适当升高温度 | ||
| C. | 增大O2的浓度 | D. | 选择高效催化剂. |
9.氮的氧化物(如NO2、NO4、N2O5等)应用很广,在一定条件下可以相互转化.
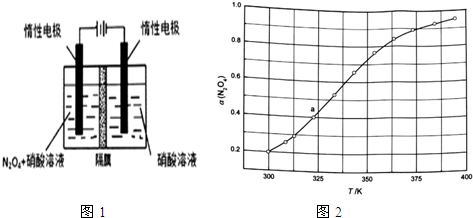
(l)从N2O5可通过电解或臭氧氧化N2O4的方法制备.电解装置如图1所示(隔膜用于阻止水分子通过),其阳极反应式为N2O4+2HNO3-2e-═2N2O5+2H+.
己知:2NO(g)+O2(g)═2NO2(g)△H1
NO(g)+O3(g)═NO2(g)+O2(g)△H2
2NO2(g)?N2O4(g)△H3
2N2O5(g)═4NO2(g)+O2(g)△H4
则反应N2O4(g)+O3(g)═N2O5(g)+O2(g)的△H=△H=△H2-$\frac{1}{2}$△H1-△H3-$\frac{1}{2}$△H4.
(2)从N2O5在一定条件下发生分解:2N2O5(g)═4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
设反应开始时体系压强为P0,第2.00min时体系压强为p,则p:p0=1.75;
1.00~3.00min内,O2的平均反应速率为0.090mol•L-1•min-1.
(3)从N2O4与NO2之间存在反应N2O4?2NO2(g).将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图1所示.
①图中a点对应温度下,已知N2O4的起始压强p0为108kPa,列式计算该温度下反应的平衡常数Kp=115.2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
②由图推测N2O4(g)?2NO2(g)是吸热反应还是放热反应,说明理由吸热反应,温度升高,α(N2O4)增加,说明平衡右移,若要提高N2O4转化率,除改变反应温度外,其他措施有减小体系压强、移出NO2(要求写出两条).
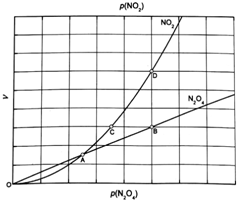
③对于反应N2O4(g)?2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1•p(N2O4),v(NO2)=k2[p(NO2)]2.其中,kl、k2是与反应及温度有关的常数.相应的速率一压强关系如图所示:一定温度下,kl、k2与平衡常数Kp的关系是kl=$\frac{1}{2}$K2.Kp,在图标出的点中,指出能表示反应达到平衡状态的点并说明理由B点与D点,满足平衡条件υ(NO2)=2υ(N2O4).
(l)从N2O5可通过电解或臭氧氧化N2O4的方法制备.电解装置如图1所示(隔膜用于阻止水分子通过),其阳极反应式为N2O4+2HNO3-2e-═2N2O5+2H+.

己知:2NO(g)+O2(g)═2NO2(g)△H1
NO(g)+O3(g)═NO2(g)+O2(g)△H2
2NO2(g)?N2O4(g)△H3
2N2O5(g)═4NO2(g)+O2(g)△H4
则反应N2O4(g)+O3(g)═N2O5(g)+O2(g)的△H=△H=△H2-$\frac{1}{2}$△H1-△H3-$\frac{1}{2}$△H4.
(2)从N2O5在一定条件下发生分解:2N2O5(g)═4NO2(g)+O2(g).某温度下测得恒容密闭容器中N2O5浓度随时间的变化如下表:
| t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| c(N2O5)/mol/L | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
1.00~3.00min内,O2的平均反应速率为0.090mol•L-1•min-1.
(3)从N2O4与NO2之间存在反应N2O4?2NO2(g).将一定量的N2O4放入恒容密闭容器中,测得其平衡转化率[a(N2O4)]随温度变化如图1所示.
①图中a点对应温度下,已知N2O4的起始压强p0为108kPa,列式计算该温度下反应的平衡常数Kp=115.2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
②由图推测N2O4(g)?2NO2(g)是吸热反应还是放热反应,说明理由吸热反应,温度升高,α(N2O4)增加,说明平衡右移,若要提高N2O4转化率,除改变反应温度外,其他措施有减小体系压强、移出NO2(要求写出两条).
③对于反应N2O4(g)?2NO2(g),在一定条件下N2O4与NO2的消耗速率与自身压强间存在关系:v(N2O4)=k1•p(N2O4),v(NO2)=k2[p(NO2)]2.其中,kl、k2是与反应及温度有关的常数.相应的速率一压强关系如图所示:一定温度下,kl、k2与平衡常数Kp的关系是kl=$\frac{1}{2}$K2.Kp,在图标出的点中,指出能表示反应达到平衡状态的点并说明理由B点与D点,满足平衡条件υ(NO2)=2υ(N2O4).

7.W、X、Y、Z、M、N六种主族元素,它们在周期表中位置如图所示,下列说法不正确的是( )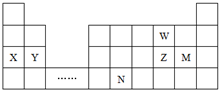

| A. | 原子半径:Y>Z>W | |
| B. | 单质的还原性:X>Y | |
| C. | 溴与元素M同主族,最高价氧化物的水化物的酸性比M的强 | |
| D. | 元素N位于金属与非金属的分界线附近,可以推断N元素的单质可作半导体材料 |
