题目内容
在铁的氧化物和氧化铝组成的混合物中,加入2mol/L硫酸溶液65mL,恰好完全反应.所得溶液中Fe2+能被标准状况下112mL氯气氧化.则原混合物中金属元素和氧元素的原子个数之比为( )
| A、5:7 | B、4:3 |
| C、3:4 | D、9:13 |
考点:有关混合物反应的计算
专题:计算题
分析:根据题意,铁的化合物中的铁元素可能含有+2价和+3价,根据氯气将亚铁离子氧化的反应,结合氯气的量可以计算亚铁离子的量,根据原子守恒和电子守恒即可计算原子个数之比.
解答:
解:硫酸的物质的量n=2mol/L×0.065L=0.13mol,所以n(H+)=0.26mol,
氯气是
=0.005mol,共失电子是0.01mol,根据反应:2Fe2++Cl2=2Fe3++2Cl-,则溶液中n(Fe2+)=0.01mol,能得电子是0.01mol,
设FeO为Xmol,Fe2O3和Al2O3为Ymol,则X+3Y=0.13,X=0.01,所以Y=0.04
所以金属原子个数是0.01+0.04×2=0.09,氧是0.01+0.04×3=0.13
即原混合物中金属元素和氧元素的原子个数之比为9:13.
故选D.
氯气是
| 0.112L |
| 22.4L/mol |
设FeO为Xmol,Fe2O3和Al2O3为Ymol,则X+3Y=0.13,X=0.01,所以Y=0.04
所以金属原子个数是0.01+0.04×2=0.09,氧是0.01+0.04×3=0.13
即原混合物中金属元素和氧元素的原子个数之比为9:13.
故选D.
点评:本题考查学生含铁化合物的性质等知识,注意守恒思想在解题中的应用,难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在标准状况下将1.92g铜粉投入一定量浓HNO3中随着铜粉的溶解,反应生成的气体颜色逐渐变浅,当铜粉完全溶解后共收集到由NO2和NO组成的混和气体1.12L,则混和气体中NO的体积为( )
| A、112mL |
| B、1008mL |
| C、224mL |
| D、336mL |
二氧化硅晶体是立体的网状结构,其结构如图所示.关于二氧化硅晶体的下列说法不正确的是( )
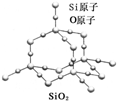

| A、晶体中Si、O原子个数比为1:2 |
| B、晶体中Si、O原子最外层都满足8电子结构 |
| C、晶体中一个硅原子含有Si-O键数目为4 |
| D、晶体中最小环上的原子数为6 |
在盛放浓硫酸的试剂瓶的标签上应印有如图警示标记中的( )
A、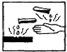 |
B、 |
C、 |
D、 |
某城市人口密度大,汽车等交通工具向大气的对流层中大量排放碳氢化合物、氮氧化物等有害物质,则下列现象最有可能发生的是( )
| A、酸雨 | B、臭氧空洞 |
| C、光化学烟雾 | D、温室效应 |
下列说法正确的是( )
| A、符合CnH2n+2通式的一定是同系物 |
| B、符合CnH2n通式的一定是同系物 |
| C、符合CnH2n-2通式的一定是同系物 |
| D、符合CnH2n-6通式的一定是同系物 |
1.00L 1.00mol?L-1 NaOH溶液与足量的稀盐酸反应,放出 57.4kJ的热量.表示该反应的中和热的热化学方程式正确的是( )
| A、NaOH+HCl═NaCl+H2O△H=+57.4kJ?mol-1 |
| B、NaOH+HCl═NaCl+H2O△H=-57.4 kJ?mol-1 |
| C、NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=+57.4 kJ?mol-1 |
| D、NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l)△H=-57.4 kJ?mol-1 |