题目内容
12.四氯化钛(T1Cl4)是制取航天航空工业材料--钛合金的重要原料.实验室以TiO2和CCl4为原料制取液态TiCl4的装置如图所示(部分夹持装詈省略).
已知:
①制取TiC14的反应原理为TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g)
②有关物质的性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 其他 |
| CCl4 | -23 | 76 | 与TiCl4互溶 |
| TiCl4 | -25 | 136 | 遇潮湿空气产生白雾,在550℃时能被氧气氧化 |
(1)仪器N的名称是圆底烧瓶,仪器A中盛装的试剂是碱石灰.
(2)检查装置气密性的方法是关闭止水夹K,在装置E中加入水浸没长导管下端,在水槽M中加入热水,装置E的长
导管口有气泡产生,移去水槽M,一段时间后,导管中形成一段水柱,则说明装置气密性
良好(或其他合理答案)
反应前通入N2的目的是排除装置中的空气,保证反应在无氧无水环境下进行
(3)装置B中热水的作用是使CCl4汽化.
(4)欲分离D中的液态混合物,所采用操作的名称是蒸馏.
(5)TiC14还可由TiO2、焦炭和氯气在加热条件下反应制得,同时有气体生成,请设计实验方案探究气体中是否同时含有CO和CO2两种气体:将气体先通过澄清石灰水,干燥后再通人装有灼热Cu0的玻璃管中,若澄清石灰水变浑
浊且玻璃管中有红色固体生成,则气体中同时含有CO与C02两种气体(或其他合理答
案).
分析 通过氮气将装置中空气排出,防止TiCl4被氧化,A为干燥管,干燥氮气,防止生成的TiCl4遇潮湿的气体产生白雾;B装置加热使四氯化碳挥发,C中装置在加热条件下,发生反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),CCl4、TiCl4熔点较低,D装置使这两种物质转化为液态,二者能互溶,应该采用蒸馏方法分离,E装置连接空气,应该盛放浓硫酸,干燥空气;
(1)该仪器名称是圆底烧瓶;A中盛放物质要具有吸水性,且为固体;
(2)检验装置气密性方法为:关闭止水夹K,在装置E中加入水浸没长导管下端,在水槽M中加入热水,装置E的长导管口有气泡产生,移去水槽M,一段时间后,导管中形成一段水柱,则说明装置气密性
良好;
TiCl4易被氧气氧化,所以制备该物质时要防止被氧气氧化;
(3)常温下四氯化碳是液体,为了得到四氯化碳气体,应该将CCl4汽化;
(4)分离互溶的液体采用蒸馏方法;
(5)利用CO的还原性检验CO,利用二氧化碳和澄清石灰水反应检验二氧化碳.
解答 解:通过氮气将装置中空气排出,防止TiCl4被氧化,A为干燥管,干燥氮气,防止生成的TiCl4遇潮湿的气体产生白雾;B装置加热使四氯化碳挥发,C中装置在加热条件下,发生反应TiO2(s)+CCl4(g)$\frac{\underline{\;\;△\;\;}}{\;}$TiCl4(g)+CO2(g),CCl4、TiCl4熔点较低,D装置使这两种物质转化为液态,二者能互溶,应该采用蒸馏方法分离,E装置连接空气,应该盛放浓硫酸,干燥空气;
(1)该仪器名称是圆底烧瓶,圆底烧瓶;A中盛放物质要具有吸水性,且为固体,可以是碱石灰,
故答案为:圆底烧瓶;碱石灰(或其他合理答案);
(2)检验装置气密性方法为:关闭止水夹K,在装置E中加入水浸没长导管下端,在水槽M中加入热水,装置E的长导管口有气泡产生,移去水槽M,一段时间后,导管中形成一段水柱,则说明装置气密性
良好;
TiCl4易被氧气氧化,所以制备该物质时要防止被氧气氧化,所以要排除装置中的空气,保证该反应在无氧无水环境下进行,
故答案为:关闭止水夹K,在装置E中加入水浸没长导管下端,在水槽M中加入热水,装置E的长
导管口有气泡产生,移去水槽M,一段时间后,导管中形成一段水柱,则说明装置气密性
良好(或其他合理答案);排除装置中的空气,保证反应在无氧无水环境下进行;
(3)常温下四氯化碳是液体,为了得到四氯化碳气体,应该将CCl4汽化,所以B加热的目的是使CCl4汽化,故答案为:使CCl4汽化;
(4)互溶的溶液采用蒸馏方法分离,四氯化碳和四氯化钛互溶,应该采用蒸馏方法分离,故答案为:蒸馏;
(5)气体可能是CO或CO2或CO与CO2的混合气体,利用CO的还原性检验CO,利用二氧化碳和澄清石灰水反应检验二氧化碳,其检验方法为:将气体先通过澄清石灰水,干燥后再通人装有灼热Cu0的玻璃管中,若澄清石灰水变浑浊且玻璃管中有红色固体生成,则气体中同时含有CO与C02两种气体(或其他合理答案),
故答案为:将气体先通过澄清石灰水,干燥后再通人装有灼热Cu0的玻璃管中,若澄清石灰水变浑浊且玻璃管中有红色固体生成,则气体中同时含有CO与C02两种气体(或其他合理答案).
点评 本题考查物质制备,为高频考点,涉及物质检验、物质制备、基本实验操作、仪器使用及名称等知识点,明确实验原理及实验基本操作方法是解本题关键,注意结合实验目的解答,知道流程图中发生的反应及注意事项,题目难度不大.

 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案| A. | Mn>Cu | B. | Al>Mn | C. | Mn>Mg | D. | Mn>H |
| A. | 用加入过量铁粉的方法除去Cu(NO3) 2溶液中混有的AgNO3 | |
| B. | 用NaOH溶液除去CO2中混有的HCl气体 | |
| C. | 向某无色未知溶液中加入BaCl2溶液,以检验未知溶液中是否含有SO42- | |
| D. | 用紫色石蕊试液、BaCl2溶液,将盐酸、硫酸、硫酸钠、氢氧化钠和硝酸钾五种无色溶液鉴别开 |
| A. | 大力发展太阳能和风力发电机可缓解电力紧张问题 | |
| B. | 将地沟油回收加工为燃料油,提高资源的利用率 | |
| C. | 推广使用一次性木筷,减少疾病传染 | |
| D. | 推广使用电动汽车、天然气汽车等环保公共交通工具 |
| 加入的物质 | 结论 | |
| A | 100mL 2mol•L-1H2SO4 | 反应结束后,c(Na+)=c(SO42-) |
| B | 0.20molCaO | 溶液中$\frac{c(O{H}^{-})}{c(HC{O}_{3}^{-})}$增大 |
| C | 200mL H2O | 由水电离出的c(H+)•c(OH-)不变 |
| D | 0.4molNaHSO4固体 | 反应完全后,溶液pH减小,c(Na+)不变 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 气体的摩尔体积约为22.4L•mol-1 | |
| B. | 在标准状况下,1mol任何物质所占的体积都约为22.4L | |
| C. | HNO3的摩尔质量是63g | |
| D. | 硫酸和磷酸的摩尔质量相等,都是98g/mol |
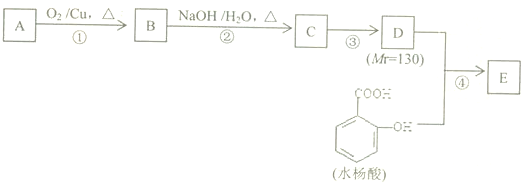
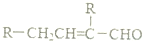
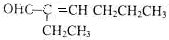 ,若要检验C中所含官能团,一次取样检验,按使用的先后顺序写出所用试剂用银氨溶液先检验醛基,再加稀盐酸使溶液呈酸性后,加溴水检验碳碳双键.
,若要检验C中所含官能团,一次取样检验,按使用的先后顺序写出所用试剂用银氨溶液先检验醛基,再加稀盐酸使溶液呈酸性后,加溴水检验碳碳双键. .
. 甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.
甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质.