题目内容
如图是从苯酚的乙醇溶液中分离回收苯酚的操作流程图:
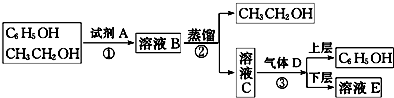
根据图示完成下列问题:
(1)试剂A的化学式为 .
(2)步骤③的操作名称为 .
(3)写出C+D-→E+C6H5OH的化学方程式: .

根据图示完成下列问题:
(1)试剂A的化学式为
(2)步骤③的操作名称为
(3)写出C+D-→E+C6H5OH的化学方程式:
考点:"三废"处理与环境保护,物质的分离、提纯和除杂
专题:实验设计题
分析:由于NaOH能与苯酚反应生成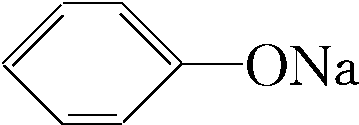 而不与C2H5OH反应,故可以加入A为NaOH(或KOH等强碱)溶液,B为
而不与C2H5OH反应,故可以加入A为NaOH(或KOH等强碱)溶液,B为 与C2H5OH混合溶液;利用C2H5OH与苯酚钠有较大的沸点差,蒸馏出乙醇,所以C为
与C2H5OH混合溶液;利用C2H5OH与苯酚钠有较大的沸点差,蒸馏出乙醇,所以C为 ;再向所得
;再向所得 的溶液中通入足量的CO2,使苯酚钠转化为苯酚,通过分液操作使之分离,据此分析解答.
的溶液中通入足量的CO2,使苯酚钠转化为苯酚,通过分液操作使之分离,据此分析解答.
 而不与C2H5OH反应,故可以加入A为NaOH(或KOH等强碱)溶液,B为
而不与C2H5OH反应,故可以加入A为NaOH(或KOH等强碱)溶液,B为 与C2H5OH混合溶液;利用C2H5OH与苯酚钠有较大的沸点差,蒸馏出乙醇,所以C为
与C2H5OH混合溶液;利用C2H5OH与苯酚钠有较大的沸点差,蒸馏出乙醇,所以C为 ;再向所得
;再向所得 的溶液中通入足量的CO2,使苯酚钠转化为苯酚,通过分液操作使之分离,据此分析解答.
的溶液中通入足量的CO2,使苯酚钠转化为苯酚,通过分液操作使之分离,据此分析解答.解答:
解:由于NaOH能与苯酚反应生成 而不与C2H5OH反应,故可以加入A为NaOH(或KOH等强碱)溶液,B为
而不与C2H5OH反应,故可以加入A为NaOH(或KOH等强碱)溶液,B为 与C2H5OH混合溶液;利用C2H5OH与苯酚钠有较大的沸点差,蒸馏出乙醇,所以C为
与C2H5OH混合溶液;利用C2H5OH与苯酚钠有较大的沸点差,蒸馏出乙醇,所以C为 ;再向所得
;再向所得 的溶液中通入足量的CO2,使苯酚钠转化为苯酚,通过分液操作使之分离,
的溶液中通入足量的CO2,使苯酚钠转化为苯酚,通过分液操作使之分离,
(1)根据以上分析,A的化学式为NaOH(或KOH),故答案为:NaOH(或KOH);
(2)根据以上分析,步骤③的操作名称为分液,故答案为:分液;
(3)C+D-→E+C6H5OH的化学方程式为: +CO2+H2O→NaHCO3+
+CO2+H2O→NaHCO3+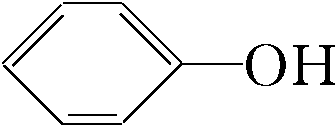 ,
,
故答案为: +CO2+H2O→NaHCO3+
+CO2+H2O→NaHCO3+ .
.
 而不与C2H5OH反应,故可以加入A为NaOH(或KOH等强碱)溶液,B为
而不与C2H5OH反应,故可以加入A为NaOH(或KOH等强碱)溶液,B为 与C2H5OH混合溶液;利用C2H5OH与苯酚钠有较大的沸点差,蒸馏出乙醇,所以C为
与C2H5OH混合溶液;利用C2H5OH与苯酚钠有较大的沸点差,蒸馏出乙醇,所以C为 ;再向所得
;再向所得 的溶液中通入足量的CO2,使苯酚钠转化为苯酚,通过分液操作使之分离,
的溶液中通入足量的CO2,使苯酚钠转化为苯酚,通过分液操作使之分离,(1)根据以上分析,A的化学式为NaOH(或KOH),故答案为:NaOH(或KOH);
(2)根据以上分析,步骤③的操作名称为分液,故答案为:分液;
(3)C+D-→E+C6H5OH的化学方程式为:
 +CO2+H2O→NaHCO3+
+CO2+H2O→NaHCO3+ ,
,故答案为:
 +CO2+H2O→NaHCO3+
+CO2+H2O→NaHCO3+ .
.
点评:本题考查物质的分离和提纯,侧重于苯酚的性质的考查,题目难度不大,注意把握常见物质的分离操作.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
某有机物样品的质谱图如图所示,则该有机物可能是( )
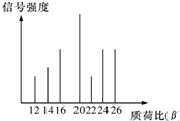

| A、甲醇 | B、甲烷 | C、乙醇 | D、乙炔 |
下列关于镁及其化合物的叙述不正确的是( )
| A、把镁粉投入氯化铁溶液中,常温下不会有氢气放出 |
| B、工业上通常用煅烧菱镁矿来制取氧化镁 |
| C、镁的主要用途是用于制造合金和照明弹 |
| D、食盐中如含氯化镁就易潮解 |
合金是指两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.分析下表中的数据,不能形成合金的是( )
| Na | Cu | Al | Fe | |
| 熔点/℃ | 97.8 | 1083 | 660 | 1535 |
| 沸点/℃ | 883 | 2567 | 2467 | 2750 |
| A、Cu和Al |
| B、Fe和Cu |
| C、Cu和Na |
| D、Al和Na |
下列判断正确的是( )
| A、在水电离出来的c(H+)=1×10-13mol/L的溶液中Fe3+、NH4+、NO3-一定不能大量共存 |
| B、AlCl3溶液蒸干后得到的固体是AlCl3 |
| C、在0.1 mol/L CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) |
| D、pH=3的醋酸溶液跟pH=11的氢氧化钡溶液等体积混合后,溶液pH=7 |
随着矿石能源的紧缺,电动汽车将成为汽车市场的主角.电动汽车以LiFePO4电池作为动力,LiFePO4电池具有稳定性高、安全、对环境友好等优点.电池反应为:LiFePO4
FePO4+Li,负极材料是石墨,电解质为含Li+的导电固体.下列有关LiFePO4电池说法正确的是( )
| 充电 |
| 放电 |
| A、放电时电池内部Li+向负极移动 |
| B、电池的负材料为Li |
| C、放电过程中,电池正极材料发生氧化反应 |
| D、充电时阴极反应为:FePO4+Li++e-═LiFePO4 |