题目内容
有关化学键和化合物的叙述不正确的是
A.盐酸中含有H+和Cl-,所以HCl是离子化合物
B.Na2O2中含有离子键和非极性共价键
C.完全由非金属元素组成的化合物可能是离子化合物
D.双原子或多原子的单质分子中均存在化学键
A
【解析】
试题分析:A、盐酸中含有H+和Cl-,但HCl是共价化合物,故A错误;B、Na2O2中钠离子和过氧根离子之间存在离子键,氧原子和氧原子之间存在非极性共价键,故B正确;C、完全由非金属元素组成的化合物可能是离子化合物,如铵盐,故C正确;D、双原子或多原子的单质分子中均存在化学键,稀有气体中没有化学键,故D正确。
考点:本题考查化学键与化合物。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列有关实验现象和解释或结论都正确的是
选项 | 实验操作 | 实验现象 | 解释或结论 |
A | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2 △H<0 |
B | 将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡 | 下层分别呈无色 和紫红色 | 还原性:I- >Br- >Fe2+ |
C | 某钾盐溶于盐酸,产生无色无味气体,通过澄清石灰水 | 有白色沉淀出现 | 该钾盐是K2CO3 |
D | 把SO2通入紫色石蕊试液中 | 紫色褪去 | SO2具有漂白性 |
 、NO
、NO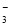
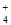 、Na+、SiO
、Na+、SiO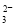 、HCO
、HCO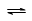 CO(g)+H2(g);
CO(g)+H2(g); H2(g)+CO2(g)。
H2(g)+CO2(g)。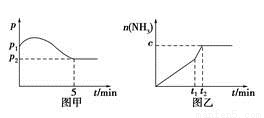
 CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如下图所示:0~4 s内,用H2 (g)表示的反应速率为____________,用CO(g)表示的反应速率为__________。
CO(g)+3H2(g)制备CO和H2。在一定条件下1 L的密闭容器中充入0.3 mol H2O和0.2 mol CH4,测得H2(g)和CH4(g)的物质的量浓度随时间变化曲线如下图所示:0~4 s内,用H2 (g)表示的反应速率为____________,用CO(g)表示的反应速率为__________。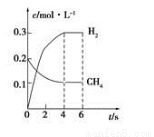
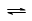 N2O4的
N2O4的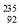 U是一种重要的核燃料,这里的“235”是指该原子的
U是一种重要的核燃料,这里的“235”是指该原子的