题目内容
4.4.6克的钠均分为二份,一份直接加入水中后配成1L溶液,另一份放在空气中加热燃烧生成过氧化钠后再溶于水中配成1L溶液,所得溶液浓度分别为a mol•L-1和bmol•L-1,则a与b的关系为( )| A. | a=b | B. | a=2b | C. | 2a=b | D. | 以上都不对 |
分析 4.6克的钠均分为二份,由Na元素守恒可知,最终所得溶液溶质均含等量的NaOH,结合c=$\frac{n}{V}$来解答.
解答 解:4.6克的钠均分为二份,一份直接加入水中后配成1L溶液,另一份放在空气中加热燃烧生成过氧化钠后再溶于水中配成1L溶液,
由Na元素守恒可知,两份溶液中NaOH的物质的量相同,且溶液体积均为1L,由c=$\frac{n}{V}$可知,则a=b,
故选A.
点评 本题考查物质的量浓度的计算,为高频考点,把握钠的性质及元素守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
14.向含a mol FeI2和b mol FeBr2的混合液中逐渐通入c mol Cl2,试分别填写不同当c值处于下列范围内时被氧化的离子及其物质的量.
| c值范围 | 被氧化的离子符号 | 被氧化离子的物质的量/mol |
| 0<c≤a | ① | ② |
| a<c≤$\frac{3a+b}{2}$ | ③ | ④ |
| $\frac{3a+b}{2}$<c≤3$\frac{a+b}{2}$ | ⑤ | ⑥ |
12.下列说法正确的是( )
| A. | 乙烷和乙醇是同系物 | |
| B. | 有机化合物一定含有碳元素 | |
| C. | 苯和甲苯都属于饱和烃 | |
| D. | 含有碳元素的化合物一定是有机化合物 |
19.用NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 标准状况下,6.72LO2和N2的混合气体含有的原子数为0.6NA | |
| B. | 通常状况下,8g O2和O3的混合气体含有的分子数是0.5NA | |
| C. | 常温常压下,2mol/L的100mL MgCl2溶液中,含有Cl- 个数为0.4NA | |
| D. | 标准状况下,11.2L He分子数为0.5NA |
16. 一定温度下,在冰醋酸加水稀释的过程中,溶液的导电能力(I)随着加入水的体积V变化的曲线如图所示.下列说法正确的是( )
一定温度下,在冰醋酸加水稀释的过程中,溶液的导电能力(I)随着加入水的体积V变化的曲线如图所示.下列说法正确的是( )
 一定温度下,在冰醋酸加水稀释的过程中,溶液的导电能力(I)随着加入水的体积V变化的曲线如图所示.下列说法正确的是( )
一定温度下,在冰醋酸加水稀释的过程中,溶液的导电能力(I)随着加入水的体积V变化的曲线如图所示.下列说法正确的是( )| A. | a、c两点pH不同 | |
| B. | 向c溶液中加水,溶液中所有离子浓度都减小 | |
| C. | 误用湿润的pH试纸测b点pH结果偏大 | |
| D. | $\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$b点大于c点 |
13.下列说法正确的是( )
| A. | 若丙醇中的氧为188O,它与乙酸反应生成的酯的相对分子质量是104 | |
| B. | 用乙酰水杨酸 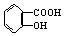 与适量NaOH溶液反应制备 与适量NaOH溶液反应制备 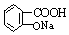 | |
| C. | 向柠檬醛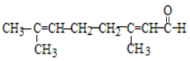 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基 | |
| D. | 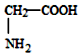 、 、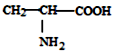 、 、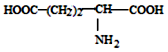 三种氨基酸脱水,最多可生成 6种二肽 三种氨基酸脱水,最多可生成 6种二肽 |
14.下列各组离子能在指定溶液中,大量共存的是( )
| A. | 含大量SO2的溶液中:NH4+、F-、HCO3-、ClO- | |
| B. | 能使淀粉碘化钾试纸变蓝的溶液:Cl-、Na+、S2-、NH4+ | |
| C. | $\frac{{k}_{w}}{c({H}^{+})}$=10-13mol/L的溶液中:Al3+、Fe3+、NO3-、ClO4- | |
| D. | 滴入KSCN溶液显红色的溶液中:NO3+、Na+、AlO2-、K+ |