题目内容
13.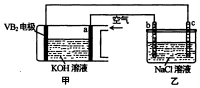 碱性硼化钒--空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5,室温下用该电池为电源,用惰性电极电解饱和氯化钠溶液,装置如图.当外电路中通过0.04mol电子时,乙装置中溶液的体积为400mL.则下列说法正确的是( )
碱性硼化钒--空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5,室温下用该电池为电源,用惰性电极电解饱和氯化钠溶液,装置如图.当外电路中通过0.04mol电子时,乙装置中溶液的体积为400mL.则下列说法正确的是( )| A. | 外电路中电子由a电极流向b电极 | |
| B. | 电极上生成气体的体积为4.48L | |
| C. | 乙装置中溶液的pH为13 | |
| D. | VB2电极发生的电极反应为:VB2+11H2O-22e-=VB2+2B2O3+22H+ |
分析 硼化钒-空气燃料电池中,VB2在负极失电子,氧气在正极上得电子,电池总反应为:4VB2+11O2=4B2O3+2V2O5,则与负极相连的c为电解池的阴极,发生还原反应,与氧气相连的b为阳极,氯离子失电子发生氧化反应,据此分析计算.
解答 解:A、外电路中电子由b电极流向a电极,故A错误;
B、状况不知,无法求体积,故B错误;
C、惰性电极电解饱和氯化钠溶液生成氢气、氯气和氢氧化钠,离子方程式:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$2OH-+H2↑+Cl2↑,当外电路中通过0.04mol电子时,生成氢氧根离子的物质的量为:0.04mol,所以c(OH-)=$\frac{0.04mol}{0.4L}$=0.1mol/L,所以溶液的pH为13,故C正确;
D、负极上是VB2失电子发生氧化反应,则VB2极发生的电极反应为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O,故D错误;
故选C.
点评 本题考查原电池及其电解池的工作原理,题目难度不大,本题注意把握电极反应式的书写,利用电子守恒计算.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列离子方程式书写正确是( )
| A. | 氯化亚铁溶液中加入稀硝酸:3Fe2++4H++NO 3-═3Fe 3++2H2O+NO↑ | |
| B. | 氧化亚铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O | |
| C. | 固体氯化钠与浓硫酸混合加热:H 2SO 4+2Cl-═SO 2↑+Cl 2↑+H 2O | |
| D. | 稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
4.如图为二维平面晶体示意图,对a、b晶体示意图所表示的化学式说法正确的是( )

| A. | a为A2X3,b为AX3 | B. | a为AX3,b为AX2 | C. | a为AX2,b为AX3 | D. | a为AX3,b为A2X3 |
1.氧、硅、铝是地壳中含量最多的三种元素,下列叙述正确的是( )
| A. | 普通玻璃、水泥成分中都含有这三种元素 | |
| B. | 自然界中存在单质硅 | |
| C. | 氧元素与另外两种元素形成的二元化合物都能与NaOH的浓溶液反应 | |
| D. | 电解熔融状态的SiO2和A12O3可以制得Si、A1,且都有氧气生成 |
8.如图为生锈了的家用铁锅,下列有关解释事实的方程式不正确的是( )


| A. | 铁锅生锈过程中有原电池反应,负极反应式是:Fe-2e-=Fe2+ | |
| B. | 铁锅生锈过程中有Fe(OH)3生成:Fe3++3H2O?Fe(OH)3+3H+ | |
| C. | 摄入体内的铁锈会在胃内产生不利于健康的Fe3+:Fe2O3+6H+═2Fe3++3H2O | |
| D. | 用醋可除去铁锈:6CH3COOH+Fe2O3═6CH3COO-+2Fe3++3H2O |
5.将H2和O2混合气体通入密闭容器中(温度为120℃),测得总压强为3.0×105Pa,点燃,冷却到原温度.若反应后总压强降为2.5×105Pa,则原来H2和O2的体积比为( )
| A. | 2:1 | B. | 5:1 | C. | 7:2 | D. | 8:1 |
12.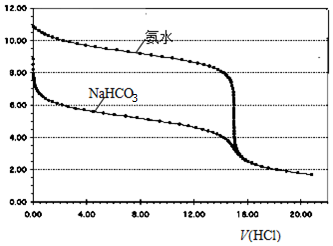 常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )
常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )
 常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )
常温下,浓度均为0.100mol•L-1、体积均为15.00mL的氨水和NaHCO3溶液分别用0.100mol•L-1HCl溶液滴定,其滴定曲线如图所示:当两溶液中均滴入相同体积的HCl溶液时,相应的两溶液中微粒的物质的量浓度关系一定正确的是( )| A. | 当V(HCl)=0 mL时,c(NH3•H2O)=c(HCO3-) | |
| B. | 当V(HCl)=4.00 mL时,c(NH4+)>c(NH3•H2O)>c(HCO3-)>c(CO32-) | |
| C. | 当V(HCl)=8.00 mL时,c(Na+)<c(NH4+)+c(HCO3-)+2c(CO32-) | |
| D. | 当V(HCl)=15.00 mL时,c(Na+)=c(NH4+)+c(NH3•H2O) |
9.二甲苯的苯环上有一个氢原子被取代后溴代物有六种同分异构体,它们的熔点如表所示:
下列说法正确的是( )
| 二甲苯一溴水代物熔点(℃) | 234 | 206 | 213.8 | 204 | 211.5 | 205 |
| 对应二甲苯熔点(℃) | 13.3 | -47.9 | -25.2 | -47.9 | -25.2 | -47.9 |
| A. | 熔点234℃的一溴二甲苯是一溴对二甲苯 | |
| B. | 熔点204℃的一溴二甲苯是一溴邻二甲苯 | |
| C. | 熔点-47.9℃的二甲苯是对二甲苯 | |
| D. | 熔点205℃的一溴二甲苯是一溴间二甲苯 |
10.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | C2H4和C3H6的混合物的质量为a g,所含碳氢键数目为aNA/7 | |
| B. | 1.0 L 1.0 mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| C. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| D. | 1 mol的羟基与1 mol的氢氧根离子所含电子数均为9NA |