题目内容
16.下列表示正确的是( )| A. | 醋酸的结构式:CH3COOH | B. | 乙炔分子的最简式:CH | ||
| C. | CCl4的球棍模型: | D. | H2O的电子式: |
分析 A.结构式中所有的共价键都需要用短线连接;
B.最简式为有机物中各种原子的个数最简比;
C.四氯化碳分子中氯原子体积大于碳原子,化学键用短线表示;
D.水为共价化合物,分子中不存在阴阳离子;
解答 解:A.醋酸的结构简式为CH3COOH,将所有共价键用短线表示即为醋酸的结构式,醋酸正确的结构式为: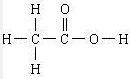 ,故A错误;
,故A错误;
B.乙炔的最简式为:CH,故B正确;
C.CCl4的球棍模型为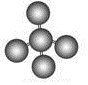 ,故C错误;
,故C错误;
D.水中存在两个氧氢键,氧原子最外层达到8电子稳定结构,水的电子式为: ,故D错误;
,故D错误;
故选B.
点评 本题考查结构式、最简式、电子式、球棍模型等化学用语的表示方法,为高频考点,题目难度中等,把握化学用语的规范应用是解答的关键.

练习册系列答案
相关题目
6.下列项目对应的结论正确的是( )
| 选项 | 项目 | 结论 |
| A | 三种有机化合物:乙烷、氯乙烯、苯 | 分子内所有原子均在同一平面上 |
| B | C(CH3)4的二氯代物数目(不考虑立体异构) | 2种 |
| C | 除去乙酸乙酯中残留的乙酸 | 可用氢氧化钠溶液 |
| D | 乙醇直接转化为乙酸,油脂水解 | 均属于取代反应 |
| A. | A | B. | B | C. | C | D. | D |
7.下列有关化学反应能量变化的叙述中正确的是( )
①燃烧反应一定是放热反应
②只要是在点燃条件下进行的反应就一定是吸热反应
③只要是在常温常压下进行的反应就一定是放热反应
④化合反应、中和反应都是放热反应,分解反应都是吸热反应
⑤如果反应物的总能量低于生成物的总能量,该反应一定是吸热反应.
①燃烧反应一定是放热反应
②只要是在点燃条件下进行的反应就一定是吸热反应
③只要是在常温常压下进行的反应就一定是放热反应
④化合反应、中和反应都是放热反应,分解反应都是吸热反应
⑤如果反应物的总能量低于生成物的总能量,该反应一定是吸热反应.
| A. | ①⑤ | B. | ④⑤ | C. | ③⑤ | D. | ①②③ |
4. “一碳化学”的重要反应CO(g)+2H2(g)?CH3OH(g)的过程能量情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
“一碳化学”的重要反应CO(g)+2H2(g)?CH3OH(g)的过程能量情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
 “一碳化学”的重要反应CO(g)+2H2(g)?CH3OH(g)的过程能量情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )
“一碳化学”的重要反应CO(g)+2H2(g)?CH3OH(g)的过程能量情况如图所示,曲线Ⅰ和曲线Ⅱ分别表示不使用催化剂和使用催化剂的两种情况.下列判断正确的是( )| A. | 曲线I的反应热比曲线II高 | |
| B. | 曲线I的反应速率比曲线II快 | |
| C. | 该反应的活化能为+91 kJ•mol-1 | |
| D. | 如果该反应生成液态CH3OH,则△H减小 |
11.仪器名称为“蒸馏烧瓶”的是( )
| A. |  | B. |  | C. |  | D. |  |
1.已知:X(g)+2Y(g)?3Z(g)△H=-a kJ•molˉ1(a>0).下列说法不正确的是( )
| A. | 0.1 mol X和0.2 mol Y充分反应生成Z,放出能量一定小于0.1 a kJ | |
| B. | Y的起始浓度不能为零,平衡浓度也不能为零 | |
| C. | 在其他条件不变的情况下,降低反应温度,正、逆反应速率均减小,平衡会发生移动 | |
| D. | 当反应达到平衡状态时,一定存在3v(Y)正=2v(Z)逆 |
8.H2与ICl的反应分①、②两步进行,其能量曲线如图所示,下列有关说法不正确的是( )

| A. | 反应②比①要容易发生是因为反应②活化能大 | |
| B. | 反应①和②均为放热反应 | |
| C. | H2(g)+2ICl(g)=I2(g)+2HCl(g)△H=-218 kJ•molˉ1 | |
| D. | 反应①和②均为氧化还原反应 |
12.CsIBr2是一种碱金属元素的多卤化物,有关该物质的说法正确的是( )
| A. | Cs显+3价,I、Br均显-1价 | B. | Cs显+1价,Br显+1价,I显-1价 | ||
| C. | CsIBr2具有较强的氧化性 | D. | CsIBr2不能与氯水反应 |
13.氢氧燃料电池已用于航于飞机.以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:
2H2+4OH--4e-=4H2O
O2+2H2O+4e-=4OH-
据此判断,下列说法中错误是( )
2H2+4OH--4e-=4H2O
O2+2H2O+4e-=4OH-
据此判断,下列说法中错误是( )
| A. | H2在负极发生氧化反应 | |
| B. | 燃料电池的能量转化率可达100% | |
| C. | 产物为无污染的水,属于环境友好电池 | |
| D. | 供电时的总反应为:2H2+O2=2H2O |