题目内容
6.Fe、Mg、Al、Cu四种金属,若两两混合,取26g混合物与足量的稀H2SO4作用,产生11.2L H2(标准状况),此混合物可能的组合方式最多有( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
分析 混合物26g与足量稀硫酸反应,产生标况下H211.2L,氢气物质的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,26g金属提供电子物质的量为0.5mol×2=1mol,故提供1mol电子需要金属的平均质量为26g,计算各金属提供1mol电子需要的质量,结合平均量进行解答.
解答 解:混合物26g与足量稀硫酸反应,产生标况下H211.2L,氢气物质的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,26g金属提供电子物质的量为0.5mol×2=1mol,故提供1mol电子需要金属的平均质量为26g,
Fe在反应中表现+2价,提供1mol电子需要Fe的质量为56g×$\frac{1mol}{2}$=28g,
Mg在反应中表现+2价,提供1mol电子需要Mg的质量为24g×$\frac{1mol}{2}$=12g,
Al在反应中表现+3价,提供1mol电子需要Al的质量为27g×$\frac{1mol}{3}$=9g,
Cu不稀硫酸反应产生氢气,提供1mol电子需要Cu的质量为无穷大,
故两两混合,可能的组合为:Cu与Mg、Cu与Al、Fe与Mg、Fe与Al,共4种,
故选C.
点评 本题考查混合物的有关计算,题目难度中等,注意平均值与极限法相结合的利用,从而简化计算,注意若有不反应的金属应视作需金属质量无穷大,试题培养了学生的化学计算能力.

练习册系列答案
 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案
相关题目
17.短周期元素A,B,C,D在周期表中的位置如图所示,E2+与D的简单阴离子有相同的电子层结构,D元素原子的次外层电子数等于其他层电子数之和,则下列说法正确的是( )
| A | B | C |
| D |
| A. | C的非金属性最强,可与E元素形成共价化合物 | |
| B. | 元素D可形成三种价态的酸,且酸根离子均能促进水的电离 | |
| C. | 原子半径由大到小的排列顺序为:E>D>B>A>C | |
| D. | C、D元素形成的最简单的氢化物的热稳定性:D<C |
11.中草药秦皮中含有的七叶树内酯(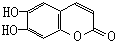 )具有抗癌作用.下列关于七叶树内酯的叙述中不正确的是( )
)具有抗癌作用.下列关于七叶树内酯的叙述中不正确的是( )
 )具有抗癌作用.下列关于七叶树内酯的叙述中不正确的是( )
)具有抗癌作用.下列关于七叶树内酯的叙述中不正确的是( )| A. | 能被KMnO4酸性溶液氧化 | |
| B. | 既可以看成酚类化合物又可看成酯类化合物 | |
| C. | 能与银氨溶液发生银镜反应 | |
| D. | 1 mol该物质最多与3 mol Br2 发生反应 |
18.只含C、H、O三种元素的有机物,在空气中燃烧时消耗的O2和生成的CO2的体积比是1:2,在这类有机物中( )
| A. | 相对分子质量最小的化合物分子式是CH2O | |
| B. | 相对分子质量最小的化合物分子式是C2H2O | |
| C. | 含相同碳原子数的各化合物,其相对分子质量之差是16的整数倍 | |
| D. | 含相同碳原子数的各化合物,其相对分子质量之差是18的整数倍 |
15.NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,0.1molC8H18所含有的共价键数目为2.5NA | |
| B. | 1L 1 mol•L-1 FeCl3溶液完全水解产生的Fe(OH)3胶体粒子数为NA | |
| C. | 氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA | |
| D. | 28.6gNa2CO3•10H2O溶于水配成1L溶液,该溶液中阴离子数目为0.1NA |
16.将甲、乙两种有机混合物在常温常压下分离,已知它们的物理性质如下:
则采用的分离方法是( )
| 物质 | 密度(g/ml-3) | 沸点(℃) | 水溶性 | 溶解性 |
| 甲 | 0.7893 | 78.5 | 溶 | 溶于乙 |
| 乙 | 1.220 | 100.7 | 溶 | 溶于甲 |
| A. | 分液 | B. | 蒸馏 | C. | 干馏 | D. | 萃取 |
 煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题:
煤的干馏是煤气化的重要方法,也是煤综合利用最“古老”的、最简单的方法.某实验小组根据教材习题设计了煤干馏实验,装置如图所示.实验时,取约2-3g的煤粒,在研体中研磨至粉末状态;用药匙将煤粉放入试管中,在具支试管中加入2mL水,按照如图所示安装好装置;点燃酒精灯,对试管预热后再集中受热,待具支试管中气泡产生的速度均匀后,在具支试管口收集气体,并用明火靠近具支试管口,可以观察到产生的气体能够燃烧.根据上述实验回答下列问题: +HNO3$→_{△}^{浓硫酸}$
+HNO3$→_{△}^{浓硫酸}$ +H2O;
+H2O;
 .
.