题目内容
4.实验室配制FeCl3的溶液时,常将固体FeCl3先溶于盐酸中,然后再用蒸馏水稀释到所需的浓度.分析 FeCl3为强酸弱碱盐,铁离子水解而使其溶液呈酸性,为防止其水解,在配制氯化铁溶液时常将FeCl3固体先溶于盐酸,由此分析解答.
解答 解:FeCl3为强酸弱碱盐,铁离子水解而使其溶液呈酸性,水解离子反应方程式为Fe3++3H2O?Fe(OH)3+3H+,根据方程式知,为防止铁离子水解,在配制氯化铁溶液时常将FeCl3固体先溶于稀盐酸中,故答案为:盐酸.
点评 本题考查了盐类水解,根据“谁强谁显性、谁弱谁水解”的规律来分析氯化铁溶液酸碱性,再结合盐类水解的影响因素来分析解答,题目难度不大.

练习册系列答案
相关题目
17.下列相关实验不能达到预期目的是( )
| 相关实验 | 预期目的 | |
| A | 向少量燃尽火柴头的浸泡液中滴加足量稀HNO3、AgNO3 | 验证火柴头含有氯元素 |
| B | 试样加水溶解后,再加入足量Ba(OH)2溶液,有白色沉淀生成 | 检验NaHCO3固体中是否含 Na2CO3 |
| C | 向溶液中加NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝的气体 | 证明原溶液中含有NH4+ |
| D | 两支试管中装有等体积、等浓度的H2O2溶液,向其中一支试管中加入FeCl3溶液 | 探究FeCl3溶液对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
15.若原子的最外层电子排布为ns1的元素R的叙述正确的是( )
| A. | 一定是ⅠA族元素 | |
| B. | 一定是金属元素 | |
| C. | 可能不是金属元素也可能是非金属元素 | |
| D. | 不是ⅡA族元素就是副族元素 |
12.下列叙述不正确的是( )
| A. | 热水中加入硫酸钠溶解至饱和,此时溶液的pH小于7 | |
| B. | 物质的量浓度相等的H2S和NaHS混合溶液中:2c(Na+)═c(S2-)+c(HS-)+c(H2S) | |
| C. | pH=13的强碱溶液,加水稀释后,溶液中氢离子的浓度变小 | |
| D. | 25℃时pH=9的CH3COONa溶液和pH=9的NH3•H2O溶液,溶液中由水电离产生的氢离子的浓度之比为104 |
19.碱性硼化钒(VB2)-空气电池工作时反应为:4VB2+11O2═4B2O3+2V2O5.用该电池为电源,选用惰性电极电解硫酸铜溶液,实验装置如图所示.当外电路中通过0.04mol电子时,B装置内共收集到0.448L气体(标准状况),则下列说法正确的是( )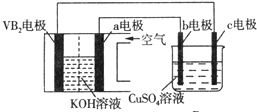

| A. | 电解过程中,c电极表面先有红色物质析出,后有气泡产生 | |
| B. | 外电路中电子由c电极流向VB2电极 | |
| C. | VB2电极发生的电极反应为:2VB2+11H2O-22e-═V2O5+2B2O3+22H+ | |
| D. | 若B装置内的液体体积为100 mL,则CuSO4溶液的物质的量浓度为0.05 mol/L |
9.关于Na2CO3和NaHCO3性质的说法不正确的是( )
| A. | 在水中的溶解性:NaHCO3<Na2CO3 | |
| B. | 相同条件下,与等浓度盐酸反应生成CO2的速率:NaHCO3<Na2CO3 | |
| C. | 等质量的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出CO2更多 | |
| D. | 等物质的量的Na2CO3和NaHCO3分别与足量盐酸反应产生的CO2质量相同 |
16.现有下列十种物质:①H2 ②铝 ③CaO ④CO2 ⑤H2SO4 ⑥Ba(OH)2 ⑦红褐色的氢氧化铁液体 ⑧氨水 ⑨稀硝酸 ⑩Al2(SO4)3
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
(2)⑩在水中的电离方程式为Al2(SO4)3=2Al3++2SO42-.
(3)少量的④通入⑥的溶液中反应的离子方程式为CO2+Ba2++2OH-=BaCO3↓+H2O
(4)②与⑨发生反应的化学方程式为:Al+4HNO3═Al(NO3)3+NO↑+2H2O,该反应的氧化剂是HNO3(填化学式),氧化剂与还原剂的物质的量之比是1:1,当有5.4g Al发生反应时,转移电子的物质的量为0.6.
(1)上述各物质按物质的分类方法填写表格的空白处(填物质编号):
| 分类标准 | 金属单质 | 氧化物 | 溶液 | 胶体 | 电解质 |
| 属于该类的物质 |
(3)少量的④通入⑥的溶液中反应的离子方程式为CO2+Ba2++2OH-=BaCO3↓+H2O
(4)②与⑨发生反应的化学方程式为:Al+4HNO3═Al(NO3)3+NO↑+2H2O,该反应的氧化剂是HNO3(填化学式),氧化剂与还原剂的物质的量之比是1:1,当有5.4g Al发生反应时,转移电子的物质的量为0.6.
13.下列离子方程式正确的是( )
| A. | 碳酸氢钠溶液与少量石灰水反应:HCO32-+Ca2++OH-═CaCO3↓+H2O | |
| B. | 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| C. | 醋酸钠溶液和盐酸混合:CH3COONa+H+═CH3COOH+Na+ | |
| D. | 铁跟氯化铁溶液反应:Fe+2Fe3+═3Fe2+ |