题目内容
5.如果BaCO3沉淀中含有0.01mol BaSO4,在1.0L次沉淀的饱和溶液中加入多少Na2CO3才能使BaSO4完全转化为BaCO3?(ksp(BaSO4)=1.1×10-10 ksp(BaCO3)=2.6×10-9)分析 据沉淀转化计算浓度,结合当Qc=c(CO32-)•c(Ba2+)≥Ksp(BaCO3 )时硫酸钡沉淀开始转化为BaCO3,据此进行计算.
解答 解:硫酸钡沉淀转化成碳酸钡沉淀的反应为:CO32-+BaSO4=BaCO3+SO42-,该反应的平衡常数K=$\frac{c(S{{O}_{4}}^{2-})}{c(C{{O}_{3}}^{2-})}$=$\frac{{K}_{sp}(BaS{O}_{4})}{{K}_{sp}(BaC{O}_{3})}$=$\frac{1.1×1{0}^{-10}}{2.6×1{0}^{-9}}$=0.0423;
已知c(SO42-)=$\frac{0.01mol}{1L}$=0.01mol/L,
则:$\frac{0.01mol/L}{c(C{{O}_{3}}^{2-})}$≤0.0423,
解得:c(CO32-)≥0.236mol/L,
1L该溶液中含有碳酸钠的物质的量为:0.238mol×1L=0.236mol,
答:在1.0L此硫酸钡饱和溶液中至少需要加入0.236mol碳酸钠,才能够使硫酸钡沉淀完全转化成碳酸钡沉淀.
点评 本题考查了难溶物溶解平衡及溶度积的有关计算,题目难度中等,明确沉淀溶解平衡的原理是解题的关键,试题侧重考查学生得到分析能力及化学计算能力.

练习册系列答案
相关题目
15.某原电池的总反应离子方程式为:2Fe3+十Fe═3Fe2+,能实现该反应的原电池是( )
| 正 极 | 负 极 | 电解质溶液 | |
| A | Cu | Fe | FeCl3 |
| B | C | Fe | Fe(NO3)3 |
| C | Fe | Zn | Fe2(SO4)3 |
| D | Ag | Fe | CuSO4 |
| A. | A | B. | B | C. | C | D. | D |
20.已知CO(g)+H2O(g)?CO2(g)+H2(g)反应的平衡常数和温度的关系如下:
回答下列问题:
(1)该反应的△H<0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的CO和0.80mol的H2O,反应初始6s内CO的平均反应速率v(CO)=0.003mol•L-1•s-1,则6s末CO2的物质的量浓度为0.018mol/L;反应达到平衡后CO的转化率为80%;
(3)判断该反应是否达到平衡状态的依据为cd(填正确选项前的字母);
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(CO)不随时间改变 d.单位时间里生成CO和H2的物质的量相等
(4)已知1000℃时,要使CO的转化率超过90%,则起始时c(H2O):c(CO)应不低于14.4;
(5)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态的K2CO3为电解质,请写出该燃料电池正极的电极反应式O2+4e-+2CO2═2CO32-;
(6)已知CO可用于制备很多物质:
2CO(g)+SO2(g)═S(g)+2CO2(g)△H=+18.0kJ•mol-1
2H2(g)+SO2(g)═S(g)+2H2O(g)△H=+90.4kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-556.0kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
请写出S(g)与O2(g)反应生成SO2(g)热化学方程式S(g)+O2(g)=SO2(g)△H=-574.0kJmol-1.
| 温度/℃ | 700 | 800 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的△H<0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的CO和0.80mol的H2O,反应初始6s内CO的平均反应速率v(CO)=0.003mol•L-1•s-1,则6s末CO2的物质的量浓度为0.018mol/L;反应达到平衡后CO的转化率为80%;
(3)判断该反应是否达到平衡状态的依据为cd(填正确选项前的字母);
a.压强不随时间改变 b.气体的密度不随时间改变
c.c(CO)不随时间改变 d.单位时间里生成CO和H2的物质的量相等
(4)已知1000℃时,要使CO的转化率超过90%,则起始时c(H2O):c(CO)应不低于14.4;
(5)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态的K2CO3为电解质,请写出该燃料电池正极的电极反应式O2+4e-+2CO2═2CO32-;
(6)已知CO可用于制备很多物质:
2CO(g)+SO2(g)═S(g)+2CO2(g)△H=+18.0kJ•mol-1
2H2(g)+SO2(g)═S(g)+2H2O(g)△H=+90.4kJ•mol-1
2CO(g)+O2(g)═2CO2(g)△H=-556.0kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
请写出S(g)与O2(g)反应生成SO2(g)热化学方程式S(g)+O2(g)=SO2(g)△H=-574.0kJmol-1.
17.下列关于配合物的说法中,正确的是( )
| A. | 配合物的外界是指配合物中的阴离子 | |
| B. | 只有过渡金属元素能形成配合物 | |
| C. | Fe(SCN)3不属于配合物 | |
| D. | Na3[AlF6]的中心原子的配位数为6 |
14.茶叶中铁元素检验可用以下步骤完成,各步骤选用实验用品不能都用到的( )

| A. | 将茶叶灼烧灰化,选用①、②和⑨ | |
| B. | 过滤得到滤液,选用④、⑤和⑦ | |
| C. | 用浓硝酸溶解茶叶灰并加蒸馏水稀释,选用④、⑥和⑦ | |
| D. | 检验滤液中的Fe3+,选用③、⑧和⑩ |
15.某无色透明溶液能与铝反应产生氢气,则此溶液中可能大量共存的离子组是( )
| A. | K+、Mg2+、NO3-、Cl- | B. | K+、Na+、HCO3-、Cl- | ||
| C. | Cu2+、Na+、SO42-、Cl- | D. | Ba2+、Na+、NO3-、Cl- |
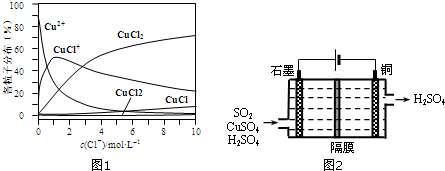
 (3)如图2所示,保持温度不变,在一定反应条件下,将2molSO2和1molO2加入甲容器中,将4molSO2和2molO2加入乙容器中,隔板K不能移动.此时控制活塞P,使乙的容积为甲的2倍.
(3)如图2所示,保持温度不变,在一定反应条件下,将2molSO2和1molO2加入甲容器中,将4molSO2和2molO2加入乙容器中,隔板K不能移动.此时控制活塞P,使乙的容积为甲的2倍.
 (1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量单位时间生成O2的体积或生成单位体积O2所需要的时间来比较;
(1)某同学通过测定O2的体积来比较H2O2的分解速率快慢,实验时可以通过测量单位时间生成O2的体积或生成单位体积O2所需要的时间来比较; 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.