题目内容
下列有关Fe(OH)3胶体的说法正确的是( )
| A、用渗析法鉴别Fe(OH)3胶体和FeCl3溶液,用丁达尔效应分离Fe(OH)3胶体和FeCl3溶液 |
| B、Fe(OH)3胶体微粒带负电荷,在通电的情况下胶体微粒向直流电源的正极移动,这种现象称为电泳 |
| C、向沸腾的蒸馏水中逐滴滴加饱和FeCl3溶液,至液体呈透明的红褐色时即得到Fe(OH)3胶体 |
| D、向沸腾的NaOH稀溶液中边滴加FeCl3饱和溶液,边用玻璃棒搅拌,然后继续煮沸制备Fe(OH)3胶体 |
考点:胶体的重要性质
专题:
分析:A.胶体具有丁达尔现象,而溶液不具有;
B.氢氧化铁胶体微粒带正电;
C.实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热;
D.实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热.
B.氢氧化铁胶体微粒带正电;
C.实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热;
D.实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热.
解答:
解:A.胶体具有丁达尔现象,而溶液不具有,则丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液;可用渗析分离Fe(OH)3胶体和FeCl3溶液,故A错误;
B.氢氧化铁胶体微粒带正电,通电时胶体微粒向直流电源负极移动,故B错误;
C.向沸腾的蒸馏水中逐滴滴入适量FeCl3饱和溶液,可制备胶体,故C正确;
D.实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热,向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液得到氢氧化铁沉淀得不到氢氧化铁胶体,故D错误.
故选C.
B.氢氧化铁胶体微粒带正电,通电时胶体微粒向直流电源负极移动,故B错误;
C.向沸腾的蒸馏水中逐滴滴入适量FeCl3饱和溶液,可制备胶体,故C正确;
D.实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热,向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液得到氢氧化铁沉淀得不到氢氧化铁胶体,故D错误.
故选C.
点评:本题考查胶体的制备与性质,为高频考点,旨在考查学生对基础知识的识记,注意基础知识的积累掌握,题目难度不大.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
下列对有机物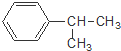 的叙述中,不正确的是( )
的叙述中,不正确的是( )
 的叙述中,不正确的是( )
的叙述中,不正确的是( )| A、它难溶于水,但易溶于苯. |
| B、它会使酸性高锰酸钾溶液褪色 |
| C、与Br2发生取代反应可生成三种一溴代物 |
| D、一定温度下可以和浓硝酸、浓硫酸的混合物发生硝化反应 |
化学概念在逻辑上存在如图关系,对下列概念的说法正确的是( )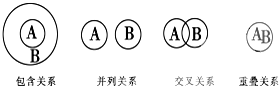

| A、化合物与电解质属于包含关系 |
| B、单质与非电解质属于包含关系 |
| C、溶液与分散系属于并列关系 |
| D、化合物与碱性氧化物属于交叉关系 |
下列溶液中,Cl-的物质的量浓度与50mL 1mol/L AlCl3溶液中Cl-物质的量浓度相等是( )
| A、100mL 1mol/LNaCl溶液 |
| B、150mL 3mol/LKCl溶液 |
| C、75mL 1mol/LMgCl2溶液 |
| D、25mL 2mol/LAlCl3溶液 |
反应4NH3+5O2?4NO+6H2O在一定体积的密闭容器中进行,30s后NO的物质的量浓度增加了3mol/L,则下列反应速率正确的是( )
| A、v (NO)=0.02 mol?(L?s)-1 |
| B、v (NO)=0.2mol?(L?s)-1 |
| C、v (NH3)=0.01 mol?(L?s)-1 |
| D、v (NH3)=0.1 mol?(L?s)-1 |
若将纳米碳均匀地分散到蒸馏水中,所形成的物质:①是溶液②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸 ⑥静置后析出黑色沉淀.其中正确的是( )
| A、①④⑥ | B、②③④ |
| C、②③⑤ | D、①③④⑥ |
关于△H的说法不正确的是( )
| A、反应的△H 由生成物与反应物的焓值差决定 |
| B、反应在恒压条件下的热效应为焓变 |
| C、某些反应的△H 可以通过实验测得 |
| D、放热反应的焓变取正值 |
下列食物属于酸性食物的是( )
| A、鸡蛋 | B、苹果 | C、葡萄 | D、西红柿 |