题目内容
为了检验某含有NaHCO3杂质的Na2CO3样品的纯度,现将w1 g 样品加热,其质量变为w2 g,则该样品的纯度(质量分数)是( )
分析:根据碳酸氢钠加热分解,而碳酸钠在加热时不反应,则利用反应前后固体的质量差来计算碳酸氢钠的质量,再计算碳酸钠样品的纯度.
解答:解:设样品中含有NaHCO3杂质的质量为x,则
2NaHCO3
Na2CO3+CO2↑+H2O?△m(减少)
2×84 106 62
x (w1g-w2g)
=
,
解得x=
,
则w(Na2CO3)=
=
,
故选A.
2NaHCO3
| ||
2×84 106 62
x (w1g-w2g)
| 2×84 |
| x |
| 62 |
| (w1g-w2g) |
解得x=
| 84(w1-w2) |
| 31 |
则w(Na2CO3)=
| w1-x |
| w1 |
| 84w2-53w1 |
| 31w1 |
故选A.
点评:本题考查学生利用反应前后的固体的质量查来进行计算,明确发生的化学反应及固体质量差的应用是解答的关键.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目

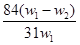


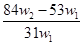 B.
B. C.
C. D.
D.