题目内容
6.请完成下列填空.(1)标准状况下,11.2L CO2的质量是22g.
(2)某BaCl2溶液100mL,其中含1.204×1023个Cl-,求n(BaCl2)=0.1mol.
(3)某学生欲用12mol•L-1浓盐酸和蒸馏水配制500mL物质的量浓度为0.60mol/L的稀盐酸.该学生需要量取25 mL上述浓盐酸进行配制.
(4)在200mL 0.5mol/L H2SO4溶液中,溶质的质量是9.8g.
(5)在相同状况下,一个空瓶,若装满N2称其质量为36g,若装满NO称其质量为40g,若装满A气体,称其质量为44g,则A的相对分子质量是32.
(6 )某固体仅由一种元素组成,其密度为5g/cm3.用X射线研究该固体的结果表明:在棱长为1×10-7 cm的立方体中含有20个原子,则此元素的相对原子质量最接近150.
分析 根据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$,以及n=cV计算相关物理量,以此解答(1)~(4);
(5)氮气体积与NO、气体A的体积相等,相同条件下三者物质的量相等,假设气体物质的量为x,氮气与NO质量之差=装满NO气体时质量-装满氮气时质量,据此计算气体的物质的量,而氧气与NO质量之差=装满氧气时质量-装满NO时质量,进而计算A的相对分子质量;
(6)根据m=ρV可计算质量,1mol原子的质量在数值上等于其相对原子质量.
解答 解:(1)n( CO2)=$\frac{11.2L}{22.4L/mol}$=0.5mol,m( CO2)=0.5mol×44g/mol=22g,故答案为:22;
(2)n(BaCl2)=$\frac{1}{2}$n(Cl-)=$\frac{1.204×1{0}^{23}}{6.02×1{0}^{23}/mol}$×$\frac{1}{2}$=0.1mol,故答案为:0.1mol;
(3)溶液稀释前后溶质的物质的量不变,某学生欲用12mol•L-1浓盐酸和蒸馏水配制500mL物质的量浓度为0.60mol/L的稀盐酸,则浓盐酸的体积为$\frac{0.5L×0.60mol/L}{12mol/L}$=0.025L=25mL,故答案为:25;
(4)n( H2SO4)=0.2L×0.5mol/L=0.1mol,m( H2SO4)=0.1mol×98g/mol=9.8g,故答案为:9.8g;
(5)氮气体积与NO、气体A的体积相等,相同条件下三者物质的量相等,假设气体物质的量为x,则:
xmol×(30g/mol-28g/mol)=40g-36g,
解得x=2,
令A的相对分子质量则y,则:
2mol×(yg/mol-30g/mol)=44g-40g,
解得y=32,
故答案为:32;
(6)20个原子的质量为 5×(1×10-7)3g=5×10-21g,所以一个原子的质量为2.5×10-22g,则NA个质量为6.02×1023×2.5×10-22=150g,故摩尔质量约为150g/mol,此元素的原子相对质量为150.
故答案为:150.
点评 本题考查了物质的量的计算,题目难度中等,涉及质量、相对分子质量的计算,明确物质的量与摩尔质量、物质的量浓度等之间的关系为解答关键,试题培养了学生的分析能力及化学计算能力.

 阅读快车系列答案
阅读快车系列答案| A. | 氧化物 | B. | 非金属 | C. | 金属或合金 | D. | 碱 |
| A. | 芳香烃就是指苯和苯的同系物 | |
| B. | 通常可从煤焦油中或通过石油的催化重整来获取芳香烃 | |
| C. | 乙苯分子中所有原子可以处于同一平面上 | |
| D. | 苯和甲苯既能发生取代反应又能发生加成反应 |
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | 稀盐酸 | 氯化钠 | 加入适量的氢氧化钠溶液 |
| B | 铜粉 | 铁粉 | 加入足量的稀盐酸溶解、过滤、洗涤 |
| C | 二氧化碳 | 一氧化碳 | 点燃 |
| D | 氯化钠溶液 | 氯化铜 | 加入过量铁粉、过滤 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 硫原子的原子结构示意图: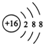 | B. | 纯碱的化学式:NaOH | ||
| C. | 原子核内有8个中子的氧原子:188O | D. | 氯化镁的电子式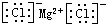 |
| A. | 胶体粒子直径在1-100nm之间 | B. | 胶体粒子带电荷 | ||
| C. | 胶体粒子能穿过滤纸 | D. | 胶体有丁达尔效应 |