题目内容
P
和[
]A
.5∶4 B.4∶3 C.5∶3 D.1∶1
答案:A

练习册系列答案
相关题目
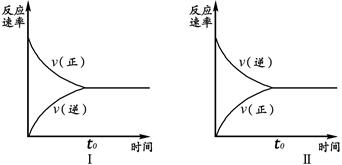
t℃时,在两个相同的密闭刚性容器(等容)中分别进行SO2和SO3相互转化的实验,反应的化学方程式为2SO2(g)+O2(g) 2SO3(g),实验Ⅰ和实验Ⅱ情况分别为图Ⅰ和图Ⅱ所示:
2SO3(g),实验Ⅰ和实验Ⅱ情况分别为图Ⅰ和图Ⅱ所示:
数据分析发现:达到平衡时,化学状态Ⅰ和化学状态Ⅱ完全相同。下列叙述不正确的是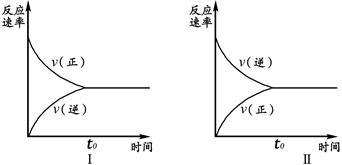
| A.若实验ⅠSO2的起始浓度为1mol/L,则实验ⅠO2的起始浓度为0.5mol/L;实验ⅡSO3的起始浓度为1mol/L. |
| B.若实验ⅠSO2的转化率为a%,则实验ⅡSO3 的转化率为1-a%。 |
| C.若起始浓度C(SO2) m mol/L,C(O2)=" n" mol/L,C(SO3)=" p" mol/L,在相同条件下进行实验,要求达到平衡时的状态与实验Ⅰ、Ⅱ完全相同,则m、n、p必须满足的条件是m/n="2" 和 m+p=1。 |
| D.维持实验Ⅰ的起始浓度和实验温度不变,改密闭刚性容器为密闭可变体积容器(等压容器)进行实验,达到化学平衡时:SO2的转化率与实验Ⅰ中SO2的转化率相比要小,但正反应速率与实验Ⅱ相比要大。 |
某小组根据工业生产原理设计如下转化关系,以获取烧碱和金属钛(Ti).
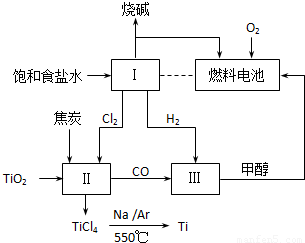
(1)燃料电池中通入氧气的电极是 (填“正”或“负”)极,电极反应式是 ;用该电池电解饱和食盐水,若消耗32g甲醇,理论上Ⅰ中可生成NaOH mol.
(2)如上图所示,理论上加入Ⅱ中的TiO2和焦炭的物质的量之比是 ;由TiCl4得到金属Ti的化学方程式是 .
(3)根据Ⅲ中合成甲醇的反应,该小组保持温度不变,在两个相同的恒容密闭容器中进行实验,有关实验数据如下:
①P1 4MPa(填“>”、“<”或“=”);
②实验Ⅰ条件下合成甲醇的热化学方程式是 .

(1)燃料电池中通入氧气的电极是 (填“正”或“负”)极,电极反应式是 ;用该电池电解饱和食盐水,若消耗32g甲醇,理论上Ⅰ中可生成NaOH mol.
(2)如上图所示,理论上加入Ⅱ中的TiO2和焦炭的物质的量之比是 ;由TiCl4得到金属Ti的化学方程式是 .
(3)根据Ⅲ中合成甲醇的反应,该小组保持温度不变,在两个相同的恒容密闭容器中进行实验,有关实验数据如下:
| 实验编号 | T/℃ | 平衡时压强P/MPa | 起始用量/mol | 平衡时CO的转化率 | 放出热量/kJ | |
| n(H2) | n(CO) | |||||
| Ⅰ | 250 | 2 | 20 | 10 | 90% | a |
| Ⅱ | 250 | P1 | 40 | 20 | c | b |
②实验Ⅰ条件下合成甲醇的热化学方程式是 .
 在两个体积均为1L的恒容容器a和b中模拟一碳化学合成甲醛,合成过程中的原理可表示为CO(g)+H2(g)?HCHO(g),其中容器a中使用催化剂.两容器中CO和H2的物质的量相同,均为1mol.试回答下列问题:
在两个体积均为1L的恒容容器a和b中模拟一碳化学合成甲醛,合成过程中的原理可表示为CO(g)+H2(g)?HCHO(g),其中容器a中使用催化剂.两容器中CO和H2的物质的量相同,均为1mol.试回答下列问题:
 2SO3(g),实验Ⅰ和实验Ⅱ情况分别为图Ⅰ和图Ⅱ所示:
2SO3(g),实验Ⅰ和实验Ⅱ情况分别为图Ⅰ和图Ⅱ所示: