题目内容
下列说法不正确的是( )

| A、反应物分子(或离子)间的每次碰撞是反应的先决条件 |
| B、反应物的分子的每次碰撞都能发生化学反应 |
| C、活化分子具有比普通分子更高的能量,催化剂能够减低活化能的数值 |
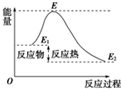
| D、活化能是活化分子的平均能量与所有分子平均能量之差,如图所示正反应的活化能为E-E1 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、反应物分子的每次碰撞不一定都能发生化学反应;
B、反应物分子间反应时必须先发生碰撞;
C、能够发生有效碰撞的分子是活化分子,活化分子具有较高能量;
D、活化能是活化分子的平均能量与所有分子平均能量之差.
B、反应物分子间反应时必须先发生碰撞;
C、能够发生有效碰撞的分子是活化分子,活化分子具有较高能量;
D、活化能是活化分子的平均能量与所有分子平均能量之差.
解答:
解:A、反应物分子间的每次碰撞是反应的先决条件,活化分子的有效碰撞是发生化学反应的充要条件,故A正确;
B、反应物分子的每次碰撞不一定能发生化学反应,只有活化分子的有效碰撞才能发生化学反应,故B错误;
C、能够发生有效碰撞的分子是活化分子,活化分子具有比普通分子更高的能量,催化剂能够减低活化能的数值,增加单位体积活化分子的百分数,故C正确;
D、活化能是活化分子的平均能量与所有分子平均能量之差,图中是E-E1,故D正确;
故选B.
B、反应物分子的每次碰撞不一定能发生化学反应,只有活化分子的有效碰撞才能发生化学反应,故B错误;
C、能够发生有效碰撞的分子是活化分子,活化分子具有比普通分子更高的能量,催化剂能够减低活化能的数值,增加单位体积活化分子的百分数,故C正确;
D、活化能是活化分子的平均能量与所有分子平均能量之差,图中是E-E1,故D正确;
故选B.
点评:本题考查了活化能对化学反应速率的影响,难度不大,会分析“能量与反应过程的图象中哪部分表示活化能,哪部分表示反应热”.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,2.24L甲醇中含有NA个碳原子 |
| B、在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4 NA |
| C、常温常压下,1mol C10H22分子中含有共价键的数目为31NA |
| D、用含有0.1molFeCl3的饱和溶液制得的氢氧化铁胶体中胶粒数等于0.1NA |
下列混合溶液中,各离子浓度的大小顺序正确的是( )
| A、10 mL 0.1 mol/L氨水与10 mL 0.1 mol/L盐酸混合,c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| B、10 mL 0.1 mol/L NH4Cl溶液与5 mL 0.2 mol/L NaOH溶液混合,c(Na+)=c(Cl-)>c(OH-)>c(H+) |
| C、10 mL 0.1 mol/L CH3COOH溶液与5 mL 0.2 mol/L NaOH溶液混合,c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
| D、10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |
对于可逆反应mA(g)+nB(s)?pC(g)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与温度T或压强p?的关系如图所示,请判断下列说法正确的是( )
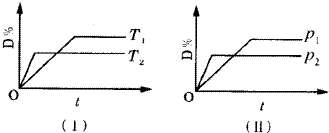

| A、降温,化学平衡向逆反应方向移动 |
| B、使用催化剂可使D%有所增加 |
| C、化学方程式中气体的化学计量数m<p+q? |
| D、B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动 |
设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A、1mol Na加热时与O2反应失去的电子数目为NA |
| B、92g N2O4和92g NO2含有的原子数均为6NA |
| C、1L 0.1mol?L-1的盐酸中,所含HCl分子数为0.1NA |
| D、标准状况下,22.4L O3中含3NA个氧原子 |
下列各方程式中,属于水解反应的是( )
| A、HCO3-+H2O?H2CO3+OH- |
| B、HCO3-+H2O?CO32-+H3O+ |
| C、HCO3-+OH-?CO32-+H2O |
| D、CO32-+H+=HCO3- |
下列说法正确的是( )
| A、炔烃可以使溴的四氯化碳溶液褪色,不能使酸性高锰酸钾溶液褪色 |
| B、某有机物燃烧只生成等物质的量的CO2和H2O,则此有机物的组成为CnH2n |
| C、鉴定溴乙烷中溴原子的存在的实验操作是:向溴乙烷中加入NaOH溶液,加热后加入AgNO3溶液 |
D、在分子 中,处于同一平面上的碳原子最多可能有12个 中,处于同一平面上的碳原子最多可能有12个 |