题目内容
氰(CN)2、硫氰(SCN)2的化学性质和卤素类似,化学上称为拟卤素〔如(SCN)2+H2O═HSCN+HSCNO〕,它们阴离子的还原性强弱为Cl-<Br-<CN-<SCN-<I-,试写出以下反应式:
①(CN)2与KOH溶液反应的化学方程式是 .
②NaBr与KSCN的混合溶液中加入(CN)2的离子方程式是: .
③已知氰(CN)2分子中各原子最外层均达到8电子稳定结构,试写出其结构式: .
①(CN)2与KOH溶液反应的化学方程式是
②NaBr与KSCN的混合溶液中加入(CN)2的离子方程式是:
③已知氰(CN)2分子中各原子最外层均达到8电子稳定结构,试写出其结构式:
考点:氧化还原反应
专题:氧化还原反应专题
分析:①根据氯气和氢氧化钾的反应书写硫氰和氢氧化钾反应方程式;
②阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-,NaBr和KSCN的混合溶液中加入足量(CN)2反应,只发生KSCN与(CN)2的反应;
③氰(CN)2分子中各原子最外层均达到8电子稳定结构,则每个碳原子形成四个共价键,每个氮原子形成三个共价键.
②阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-,NaBr和KSCN的混合溶液中加入足量(CN)2反应,只发生KSCN与(CN)2的反应;
③氰(CN)2分子中各原子最外层均达到8电子稳定结构,则每个碳原子形成四个共价键,每个氮原子形成三个共价键.
解答:
解:①由Cl2+2KOH=KCl+KClO+H2O可知,(CN)2的化学性质和卤素很相似,则(CN)2与KOH(aq)反应的化学方程式为(CN)2+2KOH=KCN+KCNO+H2O,
故答案为:(CN)2+2KOH=KCN+KCNO+H2O;
②阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-,NaBr和KSCN的混合溶液中加入足量(CN)2反应,只发生KSCN与(CN)2的反应,该反应为2SCN-+(CN)2=(SCN)2+2CN-,
故答案为:2SCN-+(CN)2=(SCN)2+2CN-;
③氰(CN)2分子中各原子最外层均达到8电子稳定结构,则每个碳原子形成四个共价键,每个氮原子形成三个共价键,所以其结构式为N≡C-C≡N,故答案为:N≡C-C≡N.
故答案为:(CN)2+2KOH=KCN+KCNO+H2O;
②阴离子的还原性强弱为:Cl-<Br-<CN-<SCN-<I-,NaBr和KSCN的混合溶液中加入足量(CN)2反应,只发生KSCN与(CN)2的反应,该反应为2SCN-+(CN)2=(SCN)2+2CN-,
故答案为:2SCN-+(CN)2=(SCN)2+2CN-;
③氰(CN)2分子中各原子最外层均达到8电子稳定结构,则每个碳原子形成四个共价键,每个氮原子形成三个共价键,所以其结构式为N≡C-C≡N,故答案为:N≡C-C≡N.
点评:本题考查了化学方程式的书写,明确还原性强弱结合知识迁移的方法分析解答,注意第二题,为易错点.

练习册系列答案
相关题目
下列有关化学用语的表示方法中正确的是( )
A、氯元素的原子结构示意图: | ||
| B、N2的结构式:N≡N | ||
C、原子核内有8个中子的氧原子:
| ||
D、二氧化碳的电子式: |
下列离子方程式书写正确的是( )
| A、泡沫灭火器的灭火原理是2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ |
| B、向硫酸铝中加入过量氨水Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| C、向硫酸亚铁酸性溶液中加入过氧化氢4Fe2++H2O2+2H+═4Fe3++2H2O |
| D、向明矾溶液中逐滴加入氢氧化钡溶液至硫酸根离子刚好沉淀完全2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
将足量Cu和含2mol溶质的浓H2SO4在加热条件下充分反应,产生SO2在标况下的体积为( )
| A、22.4L |
| B、44.8L |
| C、小于22.4L |
| D、小于44.8L |

 蒸馏是分离、提纯有机物的方法之一.装置如图:
蒸馏是分离、提纯有机物的方法之一.装置如图: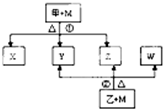 A、B、C、D、E五种元素均是短周期的主族元素,原子序数依次增大.B、E原子的最外层电子数均为其电子层数的两倍,D、E元素原子的最外层电子数相等.X、Y、Z、W均由上述元素的两种元素组成,甲、乙均由上述元素的三种元素组成.元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙).转化关系如图(反应条件略去).请回答下列问题:
A、B、C、D、E五种元素均是短周期的主族元素,原子序数依次增大.B、E原子的最外层电子数均为其电子层数的两倍,D、E元素原子的最外层电子数相等.X、Y、Z、W均由上述元素的两种元素组成,甲、乙均由上述元素的三种元素组成.元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙).转化关系如图(反应条件略去).请回答下列问题: