题目内容
M、N为短周期的两种元素,M元素原子的最外层电子数≤4,N元素原子的最外层电子数>4,下列对其中说法正确的是( )
| A、M、N可能为金属 |
| B、若M、N为同周期元素,则原子半径M<N |
| C、M、N元素的单质可能与水发生置换反应 |
| D、M、N形成的离子化合物不能体现强氧化性 |
考点:原子结构与元素周期律的关系
专题:元素周期律与元素周期表专题
分析:A.短周期元素中,原子最外层电子数大于4的元素为非金属元素;
B.同一周期元素,原子半径随着原子序数增大而减小;
C.如果M是活泼金属、N是氟气,二者都能和水发生置换反应;
D.M、N形成的离子化合物可能体现强氧化性.
B.同一周期元素,原子半径随着原子序数增大而减小;
C.如果M是活泼金属、N是氟气,二者都能和水发生置换反应;
D.M、N形成的离子化合物可能体现强氧化性.
解答:
解:A.短周期元素中,原子最外层电子数大于4的元素为非金属元素,原子最外层电子数小于4的可能是金属元素,所以M可能是金属元素,N一定是非金属元素,故A错误;
B.同一周期元素,原子半径随着原子序数增大而减小,M和N属于同一周期元素,且M原子序数小于N,则原子半径M>N,故B错误;
C.如果M是Na、N是氟气,2Na+2H2O=2NaOH+H2↑、2 F2+2H2O=4HF+O2,故C正确;
D.M、N形成的离子化合物可能体现强氧化性,如Na2O2,故D错误;
故选C.
B.同一周期元素,原子半径随着原子序数增大而减小,M和N属于同一周期元素,且M原子序数小于N,则原子半径M>N,故B错误;
C.如果M是Na、N是氟气,2Na+2H2O=2NaOH+H2↑、2 F2+2H2O=4HF+O2,故C正确;
D.M、N形成的离子化合物可能体现强氧化性,如Na2O2,故D错误;
故选C.
点评:本题考查了原子结构和元素周期律,明确物质结构和性质的关系是解本题关键,同时考查学生发散思维能力,易错选项是CD,注意C中氟气和水的反应,为易错点.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
根据图所示的各物质能量变化关系,判断下列热化学方程式正确的是( )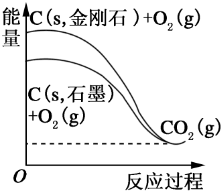

| A、C(s,金刚石)+O2(g)═CO2(g)△H1=a kJ?mol-1(a<0) |
| B、C(s,石墨)+O2(g)═CO2(g)△H2=b kJ?mol-1(b>0) |
| C、C+O2═CO2 △H3=c kJ?mol-1(c>0) |
| D、C(s,金刚石)═C(s,石墨)△H4=d kJ?mol-1(d>0) |
“可燃冰”是天然气与水相互作用形成的晶体物质,主要存在于冻土层和海底大陆架中.据测定每0.1m3固体“可燃冰”能释放出20m3甲烷气体,则下列说法中不正确的是( )
| A、“可燃冰”释放的甲烷属于烃 |
| B、“可燃冰”的分解与释放,可能会诱发海底地质灾害,加重温室效应 |
| C、“可燃冰”将成为人类的后续能源 |
| D、“可燃冰”是水变的油 |
关于容量瓶的四种叙述:
①标有使用温度;
②不宜贮存溶液;
③不能用来加热;
④使用之前要检查是否漏水.
这些叙述中正确的是( )
①标有使用温度;
②不宜贮存溶液;
③不能用来加热;
④使用之前要检查是否漏水.
这些叙述中正确的是( )
| A、①②③④ | B、②③ |
| C、①②④ | D、②③④ |
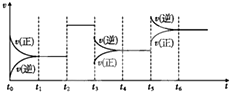 某密闭容器中发生反应:X(g)+Y(g)?3Z(g)△H<0如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )
某密闭容器中发生反应:X(g)+Y(g)?3Z(g)△H<0如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是( )| A、t2时加入了催化剂 |
| B、t3时降低了温度 |
| C、t5时增大了压强 |
| D、t4~t5时间内转化率最低 |
利用下列各组中的物质制备并收集少量相应的气体,能采用图装置的是( )

| A、过氧化氢溶液和二氧化锰制O2 |
| B、稀硝酸和铜片制NO |
| C、浓盐酸和二氧化锰制Cl2 |
| D、锌粒和稀硫酸制H2 |
按照无机物的分类方法,下列物质中前者属于碱,后者属于碱性氧化物的是( )
| A、纯碱、氧化铜 |
| B、烧碱、干冰 |
| C、熟石灰、氧化镁 |
| D、氢氧化镁、氧化铝 |
一定条件下,向2L密闭容器中加入2mol N2和10mol H2发生反应N2+3H2?2NH3,2min时测得剩余N2为1mol,此时表示的化学反应速率正确的是( )
| A、v(N2)=0.25 mol?(L?min)-1 |
| B、v(H2)=0.75 mol?(L?min)-1 |
| C、v(NH3)=1 mol?(L?min)-1 |
| D、v(NH3)=0.25mol?(L?min)-1 |
标况下,等质量的CH4和CO2比较,下列说法中不正确的是( )
| A、分子数之比为4:11 |
| B、体积比为11:4 |
| C、物质的量之比为11:4 |
| D、密度比为4:11 |