题目内容
10.一定条件下,NO2与SO2反应生成SO3和NO两种气体.将体积比为1:2的NO2、SO2气体置于密闭容器中发生上述反应,下列不能说明反应达到平衡状态的是( )| A. | 混合气体颜色保持不变 | |
| B. | 体系的平均相对分子质量保持不变 | |
| C. | NO2和SO2的体积比保持不变 | |
| D. | 每消耗1 mol SO2的同时生成1 mol NO2 |
分析 反应方程式为NO2(g)+SO2(g)?SO3(g)+NO(g),根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、混合气体颜色保持不变,说明正逆反应速率相等,故A不选;
B、反应前后气体物质的量不变,气体质量始终不变,所以体系的平均相对分子质量始终保持不变,故不能说明达平衡状态,故B选;
C、NO2和SO2按1:1的比例反应,按1:2的比例加入,反应过程中,其比值发生变化,当NO2和SO2的体积比保持不变时,说明各组分浓度不再变化,反应达到平衡状态,故C不选;
D、每消耗1 mol SO2的同时生成1 mol NO2,说明正逆反应速率相等,故D不选;
故选B.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
17.下列说法正确的是( )
| A. | 40℃时,0.005mol/LH2SO4溶液的pH为2 | |
| B. | 往氯化铁溶液中滴加氨水来制备氢氧化铁胶体 | |
| C. | 镀锌铁制品镀层受损后,铁制品易生锈 | |
| D. | 已知NaOH溶液和CH3COONH4溶液均显示中性,则两溶液中水的电离程度相同 |
1.下列对有机化合物的分类正确的是( )
| A. | 乙烯、苯、环己烷属于脂肪烃 | B. | 苯、环己烷属于芳香烃 | ||
| C. | 乙烯、乙炔属于烯烃 | D. | 环戊烷、环己烷属于环烷烃 |
18.以下转化不能通过一步反应实现的是( )
| A. | Al2O3→Al(OH)3 | B. | SiO2→SiF4 | C. | Fe→FeCl2 | D. | Na→NaOH |
15.下列有关仪器的使用,正确的是( )
| A. | 用托盘天平称取21.82g食盐 | |
| B. | 用酸式滴定管量取15.30mL 0.10mol/L H2SO4溶液 | |
| C. | 用量筒量取13.56mL盐酸 | |
| D. | 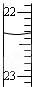 滴定达终点时,右图滴定管的正确读数为23.65mL |
19.在11.2g铁和铜组成的合金中加入过量的硝酸溶液,合金完全溶解,同时生成气体X,再向所得溶液中加入足量的NaOH溶液,生成21.4g沉淀,则下列表示X组成的选项中合理的是( )
| A. | 0.3mol NO2 | B. | 0.3mol NO、0.1mol NO2 | ||
| C. | 0.6mol NO | D. | 0.3mol NO2、0.1mol NO |
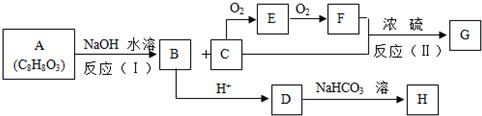
 ,E:HCHO,H:
,E:HCHO,H: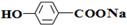 G:HCOOCH3,.
G:HCOOCH3,. .
.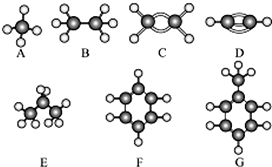 已知A~G是几种烃分子的球棍模型,据此回答下列问题:
已知A~G是几种烃分子的球棍模型,据此回答下列问题: .
. .
.