题目内容
19.2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C的反应类型属于( )| A. | 复分解反应 | B. | 置换反应 | C. | 化合反应 | D. | 分解反应 |
分析 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C为单质与化合物反应生成新单质、化合物的反应,为置换反应,以此来解答.
解答 解:A.有单质参加和生成,不属于复分解反应,故A不选;
B.为单质与化合物反应生成新单质、化合物的反应,属于置换反应,故B选;
C.生成物有两种,不是化合反应,故C不选;
D.反应物有两种,不是分解反应,故D不选;
故选B.
点评 本题考查基本反应类型,为高频考点,把握物质类别与反应分类的关系为解答的关键,侧重分析与应用能力的考查,注意基本反应类型的判断方法,题目难度不大.

练习册系列答案
 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
9.某溶液中有NH4+、Fe3+、Fe2+ 和Al3+四种离子,若向其中加入过量的氢氧化钠溶液,微热并搅拌,再加入过量盐酸,溶液中离子个数没有变化的离子是( )
| A. | NH4+ | B. | Fe3+ | C. | Fe2+ | D. | Al3+ |
10.有下列变化:①Na2CO3→Na2SiO3,②SiO2→H2SiO3,③Na2SiO3→Na2CO3,④CaO→CaSiO3,其中不能通过一步反应实现的是( )
| A. | 只有① | B. | ②④ | C. | 只有② | D. | ③④ |
7.X(g)+2Y(s)?2Z(g)△H=-aKJ/mol,一定条件下,将1molX和2molY加入2L的恒容密闭容器中,10min后测得Y的物质的量为1.4mol.下列说法正确的是( )
| A. | 10min内,X的平均反应速率为0.03mol/(L•min) | |
| B. | 若容器中的气体密度不再发生变化,说明上述反应已达平衡状态 | |
| C. | 10min后Z的浓度为0.7mol/L | |
| D. | 10min内,反应放出的热量为0.3aKJ |
4.下列物质间的转化,能通过一步反应实现的是( )
| A. | S→SO3 | B. | Fe→FeCl2 | C. | CuO→Cu(OH)2 | D. | SiO2→H2SiO3 |
9.下列过程属于“固氮”的是( )
| A. | 分离液态空气制氮气 | B. | 闪电时N2转化为NO | ||
| C. | 用NH3与CO2合成尿素 | D. | 氨氧化制硝酸 |
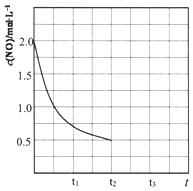 环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中的氮氧化物(NOx)、CO等有害气体,消除方法有多种.
环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中的氮氧化物(NOx)、CO等有害气体,消除方法有多种.