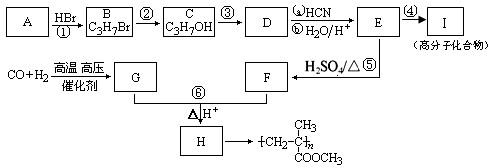
题目内容
25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )
| A、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B、将水加热,KW增大,pH不变 |
| C、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D、向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
考点:水的电离
专题:电离平衡与溶液的pH专题
分析:A.向水中加入少量稀氨水,氢氧根离子浓度增大,平衡逆向移动,c(H+)降低;
B.水的电离是吸热过程,升高温度,平衡正向移动;
C.向水中加入少量固体CH3COONa,醋酸根离子结合氢离子,c(H+)降低,平衡正向移动;
D.向水中加入少量固体硫酸氢钠,c (H+)增大,平衡逆向移动;但Kw只与温度有关.
B.水的电离是吸热过程,升高温度,平衡正向移动;
C.向水中加入少量固体CH3COONa,醋酸根离子结合氢离子,c(H+)降低,平衡正向移动;
D.向水中加入少量固体硫酸氢钠,c (H+)增大,平衡逆向移动;但Kw只与温度有关.
解答:
解:A.向水中加入少量稀氨水,氢氧根离子浓度增大,平衡逆向移动,c(H+)降低,故A错误;
B.水的电离是吸热过程,升高温度,平衡正向移动,Kw增大,氢离子浓度增大,故pH减小,故B错误;
C.向水中加入少量固体CH3COONa,醋酸根离子结合氢离子,c(H+)降低,平衡正向移动,故C错误;
D.向水中加入少量固体硫酸氢钠,c (H+)增大,平衡逆向移动;但Kw只与温度有关,故保持不变,故D正确;
故选D.
B.水的电离是吸热过程,升高温度,平衡正向移动,Kw增大,氢离子浓度增大,故pH减小,故B错误;
C.向水中加入少量固体CH3COONa,醋酸根离子结合氢离子,c(H+)降低,平衡正向移动,故C错误;
D.向水中加入少量固体硫酸氢钠,c (H+)增大,平衡逆向移动;但Kw只与温度有关,故保持不变,故D正确;
故选D.
点评:本题考查水的电离的影响因素,难度不大.要注意Kw只与温度有关.

练习册系列答案
相关题目
下列反应属于氧化反应的是( )
| A、原电池的正极 |
| B、电解池的阴极 |
| C、燃料电池的燃料 |
| D、电镀池的待镀金属 |
以CH3COOH?CH3COO-+H+的电离平衡为例:回答下列问题:
| 改变条件 | 平衡移动方向 | C(H+)C(OH-)C(CH3COO-)电离程度的变化 |
| 加入镁粉 | ||
| 升高温度 | ||
| 通入NaOH(s) | ||
| 通入HCl(g) |
某气态烃0.5mol恰好与1molHCl加成,生成物分子中的氢又可被3molCl2取代,则此气态烃可能是( )
| A、C2H2 |
| B、C2H4 |
| C、CH2=C(CH3)2 |
| D、CH≡C-CH3 |
下列物质中,不能电离出酸根离子的是( )
| A、Na2SO3 |
| B、Ba(OH)2 |
| C、KMnO4 |
| D、KCl04 |
等质量的下列物质分别与盐酸反应,消耗HCl的物质的量最少的是( )
| A、Na |
| B、Na2O2 |
| C、Na2CO3 |
| D、Ca(HCO3)2 |
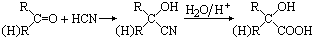 ,
,