题目内容
6.某厂生产硼砂过程中产生的固体废料.主要含有MgCO3、MgSiO3,、CaCO3、CuO、Al2O3等,获取MgCl2•6H2O工艺流程如下: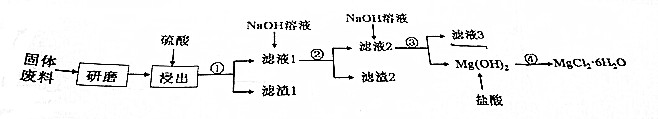
已知向滤液3中通入足量的CO2无明显现象.
下列说法不正确的是( )
| A. | “浸出”步聚中,可适当提高反应温度、增加浸出时间提高镁的浸出率 | |
| B. | 滤渣1的主要成分是CaSO4,滤液3的主要成分是Na2SO4 | |
| C. | 第1次加Na0H溶液需控制PH的目的是除去Cu2+和Al3+ | |
| D. | ①②③的操作步骤都是过滤,④的操作步骤是蒸发浓缩、冷却结晶、过滤. |
分析 A.浸出步骤中,依据影响化学平衡的因素分析判断;
B.依据MgCO3、MgSiO3,、CaCO3、CuO、Al2O3等与硫酸发生的反应及生成产物的性质;
C.依据铜离子、铝离子、镁离子沉淀时pH不同解答;
D.分离固体与液体需要采用过滤方法,从溶液中析出晶体步骤为:蒸发浓缩、冷却结晶、过滤.
解答 解:A.适当提高反应温度可以镁的浸出率,增加浸出时间不能改变化学平衡状态,所以不提高镁的浸出率,故A错误;
B.MgCO3、与硫酸反应生成可溶性硫酸镁和二氧化碳、水,MgSiO3与硫酸反应生成硅胶和可溶性硫酸镁,CaCO3与硫酸反应生成硫酸钙沉淀、二氧化碳和水,CuO与硫酸反应生成硫酸铜和水,硫酸与Al2O3反应生成可溶性硫酸铝和水,所以过滤得到的滤渣主要成分是硫酸钙,故B正确;
C.加入氢氧化钠,通过调节pH值可以使铜离子、铝离子先转化为沉淀,与镁离子分离,故C正确;
D.依据①②③操作后产物都是固体与液体可知,①②③为分离固体与液体,用过滤方法,从氯化镁溶液中得到氯化镁晶体,需要经过:蒸发浓缩、冷却结晶、过滤,故D正确;
故选:A.
点评 本题考查了物质的分离、提纯,明确工艺流程及各种物质的性质是解题关键,注意常用分离物质方法及原理,题目难度中等.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
16.下列说法正确的是( )
| A. | MgCl2晶体中的化学键是离子键 | |
| B. | 某物质在熔融态能导电,则该物质中一定含有离子键 | |
| C. | H2和Cl2两种分子中,每个原子的最外层都具有8电子稳定结构 | |
| D. | 干冰是分子晶体,其溶于水生成碳酸的过程只需克服分子间作用力 |
17.下列说法中正确的一组是( )
| A. | H2和D2互为同位素 | B. | 正丁烷和异戊烷是同系物 | ||
| C. |  和 和 互为同分异构体 互为同分异构体 | D. | 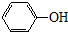 和 和 互为同系物 互为同系物 |
1.关于金属腐蚀的叙述中,正确的是( )
| A. | 金属被腐蚀的本质是:M+nH2O=M(OH)n+n/2H2↑ | |
| B. | 金属在一般情况下发生的电化学腐蚀主要是吸氧腐蚀 | |
| C. | 马口铁(镀锡)镀层破损后被腐蚀时,首先是镀层被氧化 | |
| D. | 常温下,置于空气中的金属主要发生化学腐蚀 |
11.已知lg2=0.3,在不同温度下,水达到电离平衡时c(H+)与c(OH-)的关系如图所示,下列说法中正确的是( )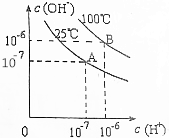

| A. | 25℃时,0.1mol/LNaOH溶液与0.1mol/L乙酸溶液等体积混合,所得溶液的pH等于7 | |
| B. | 25℃时,pH=11的氨水与pH=3的盐酸等体积混合,所得溶液的pH小于7 | |
| C. | 100℃时,pH=12的NaOH溶液aL和pH=2的H2SO4溶液bL恰好中和,则a:b=1:1 | |
| D. | 100℃时,pH=12的NaOH溶液和pH=9的NaOH溶液等体积混合,所得溶液的pH约为11.7 |
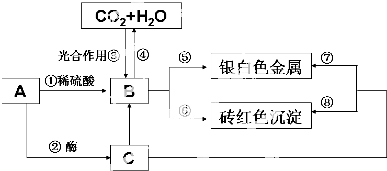
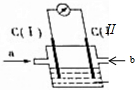 如右图所示的原电池装置中,电解质溶液为氢氧化钠溶液,a、b分别为H2、O2中的一种,C(Ⅰ)、C(Ⅱ)均为多孔石墨电极.通入气体后,发现电流表指针发生如图所示偏转.则:
如右图所示的原电池装置中,电解质溶液为氢氧化钠溶液,a、b分别为H2、O2中的一种,C(Ⅰ)、C(Ⅱ)均为多孔石墨电极.通入气体后,发现电流表指针发生如图所示偏转.则: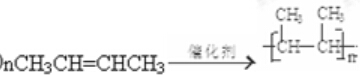
 B.Mg2+的结构示意图:
B.Mg2+的结构示意图: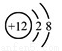
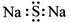 D.甲酸甲酯的结构简式:C2H4O2
D.甲酸甲酯的结构简式:C2H4O2