题目内容
20.下列实验操作或叙述正确的是(填序号)( )| A. | 乙醇中含有少量水可加入生石灰再蒸馏制得无水乙醇 | |
| B. | 将无水乙醇和浓硫酸按体积比3:1混合,加热至170℃制取乙烯 | |
| C. | 蔗糖水解用浓硫酸作催化剂 | |
| D. | 油脂皂化反应后,反应混合物中加入食盐可将肥皂分离出来 |
分析 A.水和生石灰反应,乙醇和生石灰不反应;
B.用酒精和浓硫酸制取乙烯时,浓硫酸的体积和酒精体积的比=3:1;
C.浓硫酸有脱水性,不能浓硫酸作蔗糖水解的催化剂;
D.盐析法是利用某些物质在盐溶液中的溶解度降低而分离.
解答 解:A.氧化钙可与水反应生成难挥发的氢氧化钙,乙醇和氧化钙不反应,所以可用加生石灰蒸馏的方法分离,故A正确;
B.用酒精和浓硫酸制取乙烯时,浓硫酸的体积和酒精体积的比=3:1,加热温度是170℃,如果加热温度是140℃就生成乙醚,故B错误;
C.浓硫酸有脱水性,不能浓硫酸作蔗糖水解的催化剂,否则能使蔗糖碳化,应该用稀硫酸作催化剂,故C错误;
D.向混合液中加入食盐使高级脂肪酸钠的溶解度降低而析出从而达到分离的目的,故D正确.
故选AD.
点评 本题乙醇的性质、浓硫酸的性质、油脂的性质,题目难度不大,注意根据物质的不同性质选取不同的分离方法.

练习册系列答案
相关题目
10.将几滴KSCN(SCN-是“类卤离子”,与Br-、I-等性质相似)溶液加入到含有Fe3+的酸性溶液中,溶液变成红色.将该红色溶液分为两份:
①一份中加入适量KMnO4溶液,红色褪去;
②向另一份中通入SO2,红色也褪去.
以下推测肯定不正确的是( )
①一份中加入适量KMnO4溶液,红色褪去;
②向另一份中通入SO2,红色也褪去.
以下推测肯定不正确的是( )
| A. | ②中红色褪去的原因是SO2将SCN-还原 | |
| B. | ①中红色褪去的原因是KMnO4将SCN-氧化 | |
| C. | ②中红色褪去的原因是SO2将Fe3+还原成Fe2+ | |
| D. | SCN-在适当条件下可失去电子被氧化为(SCN)2 |
11.某温度下,在1L的密闭容器中,加入1molA(g)和2molB(g)发生反应:A(g)+b B(g)?3C(g)平衡时,A、B、C的体积分数分别为30%、60%、10%.在此平衡体系中加入1molC(g),再次达到平衡后,A、B、C的体积分数不变.下列叙述不正确的是( )
| A. | b=2 | |
| B. | 两次平衡的平衡常数相同 | |
| C. | A与B的平衡转化率之比为1:2 | |
| D. | 第二次平衡时,C的浓度为0.4 mol•L-1 |
8.下列离子方程式书写正确的是( )
| A. | 硫酸亚铁加过氧化氢溶液:Fe2++H2O2+2H+═Fe3++4H2O | |
| B. | 将少量硝酸银溶液滴入氨水中:Ag++2NH3•H2O═[Ag(NH3)2]++2H2O | |
| C. | KAl(SO4)2中滴加Ba(OH)2使SO42-恰好完全沉淀:2Al3++3SO42-+3Ba2++6OH-═2Al(OH)3↓+3BaSO4↓ | |
| D. | 铝粉与NaOH的溶液反应:2Al+2OH-═AlO2-+H2↑ |
12.下列各化合物中,能发生取代、加成、消去三种反应的是( )
| A. | CH2=CH-CH2-CH2-CH3 | B. |  | ||
| C. |  | D. |  |
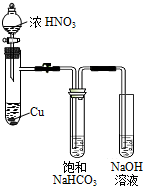 某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
某化学学习小组发现在碱性溶液中,NO2会发生如下反应:
 ,F1和F2互为同分异构体,G1和G2互为同分异构体.请填空:
,F1和F2互为同分异构体,G1和G2互为同分异构体.请填空: .
.