题目内容
19.下列离子方程式正确的是( )| A. | 钠和水反应:Na+H2O=Na++OH-+H2↑ | |
| B. | 二氧化硅和氢氧化钠溶液反应:SiO2+2OH-=SiO32-+H2O | |
| C. | 碳酸氢钡和稀硝酸反应:CO32-+2H+=CO2↑+H2O | |
| D. | 工业上电解饱和食盐水的反应:2Na++2Cl-$\frac{\underline{\;通电\;}}{\;}$2Na+Cl2↑ |
分析 A.原子个数不守恒;
B.二者反应生成硅酸钠和水;
C.碳酸氢根离子为弱酸的酸式根离子,不能拆;
D.不符合反应客观事实.
解答 解:A.钠和水反应,离子方程式:2Na+2H2O=2Na++2OH-+H2↑,故A错误;
B.二氧化硅和氢氧化钠溶液反应,离子方程式:SiO2+2OH-=SiO32-+H2O,故B正确;
C.碳酸氢钡和稀硝酸反应,离子方程式:HCO3-+H+=CO2↑+H2O,故C错误;
D.工业上电解饱和食盐水的反应,离子方程式:2H2O+2Cl-$\frac{\underline{\;通电\;}}{\;}$2OH-+Cl2↑+H2↑,故D错误;
故选:B.
点评 本题考查了离子方程式的书写,明确相关物质的性质及发生反应的实质是解题关键,注意化学式的拆分,注意反应遵循客观事实,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.漓江是我市的母亲河,保护漓江刻不容缓,下列做法中,不利于保护漓江的是( )
| A. | 将经过无害化处理的生活污水排放到漓江中 | |
| B. | 漓江沿岸不得开设造纸厂等污染企业 | |
| C. | 定期投放水生动物优化漓江生态 | |
| D. | 使用含磷洗涤剂且将洗涤后的废水排放到漓江中 |
7.配制480mL1.0mol•L-1NaNO2溶液,需称取溶质质量为( )
| A. | 13.8g | B. | 69g | C. | 34.5g | D. | 138g |
14.下列用来表示物质变化的化学用语中,正确的是( )
| A. | 钢铁发生电化腐蚀的正极反应式:Fe-2e-═Fe2+ | |
| B. | 氢氧燃料电池的负极反应式:O2+2H2O+4e-═4OH- | |
| C. | 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-═Cu2+ | |
| D. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ |
11.常温下,将某一元酸HA和NaOH溶液等体积混合,分别进行编号为①、②、③的实验,实验数据记录如下表
请回答:(1)根据①组实验情况,分析混合溶液的pH=9的原因是A-+H2O?HA+OH-.(用反应的离子方程式表示),
(2)②组情况表明,c>0.2mol•L-1(选填“>”、“<”或“=”).混合溶液中离子浓度c(A-)=c(Na+)(选填“>”、“<”或“=”)
(3)从③组实验结果分析,说明HA的电离程度>NaA的水解程度(选填“>”、“<”或“=”),离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
| 实验编号 | HA物质的量浓度(mol•L-1) | NaOH物质的量浓度(mol•L-1) | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.2 | 0.1 | pH<7 |
(2)②组情况表明,c>0.2mol•L-1(选填“>”、“<”或“=”).混合溶液中离子浓度c(A-)=c(Na+)(选填“>”、“<”或“=”)
(3)从③组实验结果分析,说明HA的电离程度>NaA的水解程度(选填“>”、“<”或“=”),离子浓度由大到小的顺序是c(A-)>c(Na+)>c(H+)>c(OH-).
8.表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)正确表示元素②在周期表中的位置第二周期第ⅣA族
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物对应的水化物是两性氢氧化物的元素是Al(填元素符号),写出它的氧化物与⑤的氢氧化物反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(4)⑧的单质有许多重要用途,写出其工业生产反应的化学方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(5)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是(用离子符号表示)O2-、Na+、Mg2+.
| 列 周期 | 1 | 2 | 13 | 14 | 15 | 16 | 17 | 18 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ |
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的化学式是HClO4,碱性最强的化合物的化学式是KOH.
(3)最高价氧化物对应的水化物是两性氢氧化物的元素是Al(填元素符号),写出它的氧化物与⑤的氢氧化物反应的离子方程式Al2O3+2OH-=2AlO2-+H2O.
(4)⑧的单质有许多重要用途,写出其工业生产反应的化学方程式2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑.
(5)③⑤⑥三元素形成的简单离子具有相同的电子层结构,它们的离子半径由大到小顺序是(用离子符号表示)O2-、Na+、Mg2+.
 .
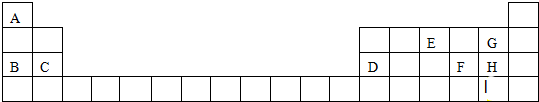
. A、B、C、D 是原子序数依次增大的短周期主族元素,A 的基态原子中电 子占据三个能级,且各个能级的电子数相等;B 的一种氧化物为红棕色气体;C 的原子半径 是短周期中最大的.D 的电负性是同周期中最大的;E 是第四周期第VIII族三种元素中原子序数 最小的元素.用元素符号回答下列问题:
A、B、C、D 是原子序数依次增大的短周期主族元素,A 的基态原子中电 子占据三个能级,且各个能级的电子数相等;B 的一种氧化物为红棕色气体;C 的原子半径 是短周期中最大的.D 的电负性是同周期中最大的;E 是第四周期第VIII族三种元素中原子序数 最小的元素.用元素符号回答下列问题: