题目内容
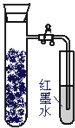 如图,向还原铁粉中加入少量的炭粉,混合均匀后,撒入内壁用NaCl溶液润湿过的具支试管中,塞紧橡皮塞.几分钟后,打开止水夹,观察到导管中水柱上升.对此过程所作的分析正确的是( )
如图,向还原铁粉中加入少量的炭粉,混合均匀后,撒入内壁用NaCl溶液润湿过的具支试管中,塞紧橡皮塞.几分钟后,打开止水夹,观察到导管中水柱上升.对此过程所作的分析正确的是( )| A、碳粉在电化学腐蚀过程中作负极 |
| B、炭粉被氧化 |
| C、发生了吸氧腐蚀 |
| D、发生了析氢腐蚀 |
考点:探究铁的吸氧腐蚀
专题:
分析:Fe、C和电解质溶液构成原电池,Fe易失电子发生氧化反应而作负极、C作正极;几分钟后,打开止水夹,观察到导管中水柱上升,说明大试管中压强减小,发生吸氧腐蚀,据此分析解答.
解答:
解:几分钟后,打开止水夹,观察到导管中水柱上升,说明大试管中压强减小,发生吸氧腐蚀,
A.发生吸氧腐蚀时,说明该装置构成原电池,Fe易失电子作负极,C作正极,故A错误;
B.该装置中C为正极,正极上氧气得电子发生还原反应,所以C不发生反应,故B错误;
C.根据以上分析知,该装置发生了吸氧腐蚀,故C正确;
D.如果发生析氢腐蚀,则大试管中气体压强增大,会导致导管中液面下降,与事实不符合,所以发生吸氧腐蚀,故D错误;
故选C.
A.发生吸氧腐蚀时,说明该装置构成原电池,Fe易失电子作负极,C作正极,故A错误;
B.该装置中C为正极,正极上氧气得电子发生还原反应,所以C不发生反应,故B错误;
C.根据以上分析知,该装置发生了吸氧腐蚀,故C正确;
D.如果发生析氢腐蚀,则大试管中气体压强增大,会导致导管中液面下降,与事实不符合,所以发生吸氧腐蚀,故D错误;
故选C.
点评:本题考查吸氧腐蚀和析氢腐蚀,明确吸氧腐蚀和析氢腐蚀区别是解本题关键,侧重考查学生分析问题能力,注意析氢腐蚀和吸氧腐蚀的条件,题目难度不大.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
关于氯气的叙述中,下列说法正确的是( )
| A、氯气是一种黄绿色、有毒的气体 |
| B、氯气可以与铁反应生成FeCl2 |
| C、氯气不能溶于水,所以可用排水法收集氯气 |
| D、氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物 |
下列关于离子的检验说法正确的是( )
| A、向某溶液中滴入足量盐酸,如观察到无色无味的气体产生,且能使澄清石灰水变浑浊,即证明溶液中必定有CO32- |
| B、向某无色溶液中加入BaCl2溶液,有白色沉淀出现,再加入稀盐酸,沉淀不消失,无法证明溶液一定含有SO42- |
| C、向某无色溶液中加入少量稀氢氧化钠溶液后,用湿润的红色石蕊试纸靠近试管口,若试纸不变蓝,则说明该溶液中无NH4+ |
| D、如透过蓝色的钴玻璃能够观察到紫色火焰,则一定有钾元素,一定不含有钠元素 |
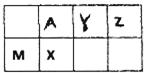 五种短周期元素在周期表中的位置如图,其中M、X、Z在地壳中的含量居前三位.
五种短周期元素在周期表中的位置如图,其中M、X、Z在地壳中的含量居前三位. 太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层.
太阳能热水器中常使用一种以镍或镍合金空心球为吸收剂的太阳能吸热涂层.