题目内容
15.下列对分子的性质的解释中,不正确的是( )| A. | 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致 | |
| B. | 乳酸[CH3CH(OH)COOH]有一对对映异构体,因为其分子中含有一个手性碳原子 | |
| C. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| D. | SiCl4的分子中硅氯键的极性比CCl4中的碳氯键强 |
分析 A.分子晶体的稳定性与化学键有关;
B. 中间碳原子上连有四个不一样的基团:氢原子、甲基、羧基和羟基,是手性碳原子;
中间碳原子上连有四个不一样的基团:氢原子、甲基、羧基和羟基,是手性碳原子;
C.极性分子的溶质极易溶于极性分子的溶剂,非极性分子的溶质极易溶于非极性分子的溶剂;
D.D、两元素电负性差越大,形成共价键极性越强.
解答 解:A.水很稳定,是因为水分子内的共价键较强的缘故,与氢键无关,氢键只影响水的熔沸点,故A错误;
B. 中间碳原子上连有四个不一样的基团:氢原子、甲基、羧基和羟基,是手性碳原子,存在对映异构即手性异构体,故B正确;
中间碳原子上连有四个不一样的基团:氢原子、甲基、羧基和羟基,是手性碳原子,存在对映异构即手性异构体,故B正确;
C.碘、四氯化碳、甲烷均是非极性分子,而水是极性溶剂,根据相似相溶原理知,碘易溶于四氯化碳,甲烷难溶于水,故C正确;
D.碳元素的电负性大于硅元素,因此Si、Cl间的电负性差别较大,Si-Cl的极性强,故D正确;
故选A.
点评 本题考查相似相溶原理、化学键与分子稳定性关系等知识点,侧重考查学生分析判断能力,注意氢键和范德华力影响分子晶体熔沸点,但分子的稳定性受化学键影响,注意二者区别,为易错点.

练习册系列答案
相关题目
6.设阿伏加德罗常数的值为NA,则下列说法正确的是( )
| A. | 标准状况下,22.4 L乙烯含有的共用电子对数为5NA | |
| B. | lmolNaHSO4中的阳离子数为2NA | |
| C. | 通常状况下,lmolNO和0.5molO2在密闭容器中混合,生成NO2分子数为NA | |
| D. | 制取漂白粉时,标准状况下22.4LC12参加反应,转移电子数为NA |
3.NaOH固体溶于水,放出大量的热量是因为( )
| A. | 发生水合过程,并且放出热量 | |
| B. | 发生扩散过程,并且放出热量 | |
| C. | 水合过程放出的热量大于扩散过程吸收的热量 | |
| D. | 扩散过程放出的热量大于水合过程吸收的热量 |
10.在反应Cl2+2NaOH═NaCl+NaClO+H2O的变化中,当产生58.5gNaCl时,转移电子总数是( )
| A. | 1.204×1024个 | B. | 6.02×1023个 | C. | 4.816×1023个 | D. | 2.408×1023个 |
20.下列措施中能减慢食品的腐败,延长其保质期的是( )
①降温冷冻 ②用盐腌制 ③加热烘干 ④适当地使用防腐剂.
①降温冷冻 ②用盐腌制 ③加热烘干 ④适当地使用防腐剂.
| A. | ①② | B. | ④ | C. | ①②④ | D. | ①②③④ |
7.化学在生产和日常生活中有着重要的应用.下列说法不正确的是( )
| A. | 工业上可用铝热反应大规模炼铁 | B. | SO2常用于纸张等植物纤维的漂白 | ||
| C. | Si是重要的半导体材料 | D. | 电解熔融MgCl2,可制得金属镁 |
4.能源、环境与生产生活和社会发展密切相关.
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.相关数据如表:
①下列情况能说明该反应一定达到平衡状态的是cd(填字母).
a.v(CO2)消耗=v(CH3OH)生成
b.气体的密度不再随时间改变
c.CO2和CH3OH的浓度之比不再随时间改变
d.气体的平均相对分子质量不再随时间改变
②其他条件不变,达到平衡后,下列不能提高H2转化率的操作是bd(填字母).
a.降低温度b.充入更多的H2c.移除甲醇d.增大容器体积
③c1=c2(填“>”“<”或“=”),a=19.6.
④该温度下反应的平衡常数K=$\frac{25}{12}$(或2.1);若甲中反应10s时达到平衡,则0~10s内甲中的平均反应速率v(H2)=0.09mol•L-1•s-1.
(2)已知反应:2NO2(红棕色)?N2O4(无色)△H<0.将一定量的NO2充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是B(填字母).
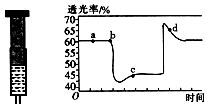
A.b点的操作是拉伸注射器
B.d点:v正<v逆
C.c点与a点相比,c(NO2)增大,c(N2O4)减小
D.若不忽略体系温度变化,且没有能量损失,则Tb>Tc.
(1)一定温度下,在两个容积均为2L的密闭容器中,分别发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.相关数据如表:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 1mol CO2(g)和3mol H2(g) | 1mol CH3OH (g)和 1mol H2O(g) |
| 平衡时c(CH3OH) | c1 | c2 |
| 平衡时能量变化 | 放出29.4kJ | 吸收a kJ |
a.v(CO2)消耗=v(CH3OH)生成
b.气体的密度不再随时间改变
c.CO2和CH3OH的浓度之比不再随时间改变
d.气体的平均相对分子质量不再随时间改变
②其他条件不变,达到平衡后,下列不能提高H2转化率的操作是bd(填字母).
a.降低温度b.充入更多的H2c.移除甲醇d.增大容器体积
③c1=c2(填“>”“<”或“=”),a=19.6.
④该温度下反应的平衡常数K=$\frac{25}{12}$(或2.1);若甲中反应10s时达到平衡,则0~10s内甲中的平均反应速率v(H2)=0.09mol•L-1•s-1.
(2)已知反应:2NO2(红棕色)?N2O4(无色)△H<0.将一定量的NO2充入注射器后封口,如图是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是B(填字母).

A.b点的操作是拉伸注射器
B.d点:v正<v逆
C.c点与a点相比,c(NO2)增大,c(N2O4)减小
D.若不忽略体系温度变化,且没有能量损失,则Tb>Tc.
5.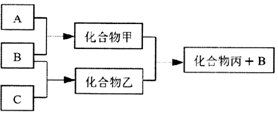 如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )
如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )
 如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )
如图所示转化关系中A、B、C均为双原子气态单质,分别由短周期主族元素X、Y、Z组成.其中单质B含共用电子对数最多,甲和丙分子中均含有10个电子.下列说法错误的是( )| A. | Z元素位于第二周期第VIA族 | |
| B. | 可用排水法收集化合物乙 | |
| C. | 元素X、Y、Z的原子半径大小关系为X<Z<Y | |
| D. | 化合物甲溶于化合物丙中,存在的微粒有5种 |
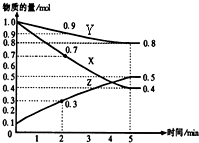 某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示:
某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示: