题目内容
15.亚硫酸钠和碘酸钾在酸性溶液里反应的化学方程式是:Na2SO3+KIO3+H2SO4=Na2SO4+K2SO4+I2+H2O,
该反应过程和机理较复杂,一般认为分为以下几步:
①IO3-+SO32-→IO2-+SO42-(慢) ②IO2-+SO32-→IO-+SO42-(快)
③5I-+6H++IO3-→3I2+3H2O(快) ④I2+SO32-+H2O→2I-+SO42-+2H2(快)
(1)根据上述条件推测,此反应的总的反应速率由①步反应决定.
(2)若预先加入淀粉溶液,由题述看必在SO32-离子消耗完时,才会使淀粉变蓝的现象产生.
分析 (1)慢反应决定反应速率;
(2)淀粉遇碘单质变蓝,由信息可知,④中消耗碘,只有SO32-完全反应时,生成的碘与淀粉作用变蓝.
解答 解:(1)只有①IO3-+SO32-→IO2-+SO42-为慢反应,决定反应速率,故答案为:①;
(2)信息可知,④中消耗碘,只有SO32-完全反应时,生成的碘与淀粉作用变蓝,则预先加入淀粉溶液,由题述看必在SO32-离子消耗完时,才会使淀粉变蓝的现象产生,故答案为:SO32-.
点评 本题考查化学反应速率机理,为高频考点,把握慢反应对反应速率的影响及淀粉的特性为解答的关键,侧重分析与应用能力的考查,注意信息的应用,题目难度不大.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
5.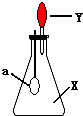 如图中,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起.气体X和液体Y不可能是( )
如图中,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起.气体X和液体Y不可能是( )
 如图中,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起.气体X和液体Y不可能是( )
如图中,锥形瓶内盛有气体X,滴管内盛有液体Y.若挤压滴管胶头,使液体Y滴入瓶中,振荡,过一会可见小气球a鼓起.气体X和液体Y不可能是( )| A. | X是NH3,Y是水 | B. | X是SO2,Y是KOH浓溶液 | ||
| C. | X是CO2,Y是稀盐酸 | D. | X是HCl,Y是NaCl稀溶液 |
3.在一定温度下,向1L密闭容器中加入1mol HI(g),发生反应2HI(g)?H2(g)+I2(g),2s 时生成0.1mol H2,则表示该时段的化学反应速率正确的是( )
| A. | v(HI)=0.8 mol•Lˉ1•sˉ1 | B. | v(I2)=0.2 mol•Lˉ1•sˉ1 | ||
| C. | v(HI)=0.1 mol•Lˉ1•minˉ1 | D. | v(H2)=0.05 mol•Lˉ1•sˉ1 |
10.锗酸铋(简称BGO)是我国研制成功的一种性能优良的闪烁晶体材料,其中锗(Ge与碳同主族)元素处于最高价态,铋元素(Bi与氮同主族)的价态与它跟氯形成某种共价氯化物所呈的价态相同,且此氯化物中铋具有8电子稳定结构.BGO的化学式是( )
| A. | Bi3Ge3O15 | B. | Bi4Ge3O12 | C. | Bi4Ge3O16 | D. | Bi3Ge3O12 |
20.某微粒用${\;}_{Z}^{A}$Rn+表示,下列关于这种微粒的叙述正确的是( )
| A. | 所含质子数Z+A | B. | 所含电子数Z+n | C. | 所含中子数 A-Z | D. | 质量数Z |
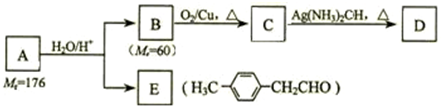
 .
. 、
、 、
、 (其中一种).
(其中一种).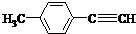 )的一条路线如下:
)的一条路线如下: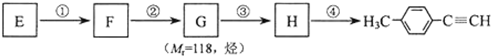
 ;
;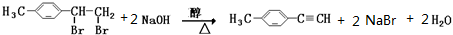 .
.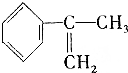 、液溴、浓硫酸和其他无机试剂,请用5个化学方程式表示下列转化过程:
、液溴、浓硫酸和其他无机试剂,请用5个化学方程式表示下列转化过程: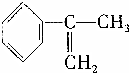 →
→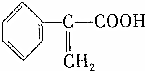
 ;
;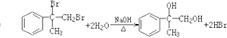 ;
; ;
; ;
;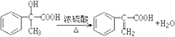 .
.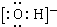 ;
;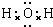 ;
;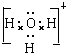 ;
;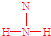 ;
;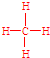 .
.