题目内容
有X、Y、Z、W四种元素,已知:
(1)它们都是短周期元素,X和Z在同一周期;在常温下W元素的单质是黄绿色气体
(2)它们可以组成:X2Z、ZY2、ZY3 化合物;
(3)ZY3与水化合生成一种常见的强酸,此强酸与X2Z发生复分解反应生成一种气体A.
根据以上推断回答下列问题:
(1)X、Y、Z、W四种元素的元素符号依次为:
(2)画出 z2-的原子结构示意图:
(3)用电子式表示X2Z的形成过程: ,用电子式表示气体A的形成过程:
(4)ZY3与水化合生成的强酸与X2Z反应的化学方程式为:
(5)A和W元素的单质反应的化学反应方程式是:
(6)X单质与Y单质在加热时得到的产物中含有的化学键有 .
(1)它们都是短周期元素,X和Z在同一周期;在常温下W元素的单质是黄绿色气体
(2)它们可以组成:X2Z、ZY2、ZY3 化合物;
(3)ZY3与水化合生成一种常见的强酸,此强酸与X2Z发生复分解反应生成一种气体A.
根据以上推断回答下列问题:
(1)X、Y、Z、W四种元素的元素符号依次为:
(2)画出 z2-的原子结构示意图:
(3)用电子式表示X2Z的形成过程:
(4)ZY3与水化合生成的强酸与X2Z反应的化学方程式为:
(5)A和W元素的单质反应的化学反应方程式是:
(6)X单质与Y单质在加热时得到的产物中含有的化学键有
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:X、Y、Z、W四种元素,它们都是短周期元素,在常温下W元素的单质是黄绿色气体,则W为Cl元素;它们可以组成:X2Z、ZY2、ZY3 化合物,而ZY3与水化合生成一种强酸,应是SO3与水反应生成硫酸,可推知Y为O、Z为S,X和Z在同一周期,由形成的化合物可知X为+1价,则X为Na,硫酸与Na2S反应可生成一种气体A为H2S,以此解答该题.
解答:
解:(1)由上述分析可知,X、Y、Z、W四种元素的元素符号依次为:Na、O、S、Cl,故答案为:Na;O;S;Cl;
(2)S2-离子核外有18个电子层,有3个电子层,各层电子数为2、8、8,结构示意图为: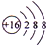 ,故答案为:
,故答案为: ;
;
(3)用电子式表示 Na2S 的形成过程为: ,用电子式表示气体H2S的形成过程为:
,用电子式表示气体H2S的形成过程为: ,故答案为:
,故答案为: ;
; ;
;
(4)硫酸与Na2S反应生成硫酸钠与硫化氢,化学方程式为:H2SO4+Na2S=Na2SO4+H2S↑,
故答案为:H2SO4+Na2S=Na2SO4+H2S↑;
(5)硫化氢与氯气反应生成S与HCl,化学反应方程式是:H2S+Cl2=S↓+2HCl,故答案为:H2S+Cl2=S↓+2HCl;
(6)Na与氧气在加热时生成过氧化钠,过氧化钠中存在钠离子与过氧根形成的离子键,过氧根之间存在非极性共价键,故答案为:离子键; 共价键.
(2)S2-离子核外有18个电子层,有3个电子层,各层电子数为2、8、8,结构示意图为:
 ,故答案为:
,故答案为: ;
;(3)用电子式表示 Na2S 的形成过程为:
 ,用电子式表示气体H2S的形成过程为:
,用电子式表示气体H2S的形成过程为: ,故答案为:
,故答案为: ;
; ;
;(4)硫酸与Na2S反应生成硫酸钠与硫化氢,化学方程式为:H2SO4+Na2S=Na2SO4+H2S↑,
故答案为:H2SO4+Na2S=Na2SO4+H2S↑;
(5)硫化氢与氯气反应生成S与HCl,化学反应方程式是:H2S+Cl2=S↓+2HCl,故答案为:H2S+Cl2=S↓+2HCl;
(6)Na与氧气在加热时生成过氧化钠,过氧化钠中存在钠离子与过氧根形成的离子键,过氧根之间存在非极性共价键,故答案为:离子键; 共价键.
点评:本题考查结构性质位置关系应用,侧重对化学用语的考查,推断元素是解题关键,注意掌握用电子式表示化学键或物质的形成过程,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
PASS是新一代高效净水剂,它由X、Y、Z、W、R五种短周期元素组成,五种元素原子序数依次增大.X原子是所有原子中半径最小的,Y、R同主族,Z、W、R同周期,Y原子的最外层电子数是次外层的3倍,Z是常见的金属,电子层数等于主族序数,W单质是人类将太阳能转变为电能的常用材料.下列说法正确的是( )
| A、Y与R形成的化合物对应的水化物一定是强酸 |
| B、如W与Y形成化合物的化学式为WY2,则WY2能与碱反应,但不能与任何酸反应 |
| C、原子半径按X、Y、W、R、Z的顺序依次增大 |
| D、R的气态氢化物一定比W的气态氢化物稳定 |
下列反应的离子方程式书写正确的是( )
| A、氯化铜溶液与铁粉反应:CuCl2+Fe═Fe2++Cu+2Cl- |
| B、稀H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ |
| C、氢氧化钡溶液与稀H2SO4反应:Ba2++SO42-═BaSO4↓ |
| D、用氢氧化钠溶液吸收氯化氢气体:H++OH-═H2O |
物质分类的依据通常有组成和性质.下列物质分类中,只考虑组成的是( )
| A、Na2SO4是钠盐、硫酸盐、正盐 |
| B、HNO3是一元酸、强酸、挥发性酸 |
| C、NaOH是一元碱、可溶性碱、强碱 |
| D、CO2是酸性氧化物、非金属氧化物、最高价氧化物 |
下列说法正确的是( )
| A、电解精炼铜时,同一时间内阳极溶解铜的质量与阴极析出铜的质量相等 |
| B、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| C、对于△H<0,△S>0的反应,不仅能自发进行,反应速率也很快 |
| D、S(g)+O2(g)=SO2(g)△H1,S(s)+O2(g)=SO2(g)△H2;则△H1<△H2 |