题目内容
9.下列变化为放热反应的是( )
| A. | 2NH4Cl+Ba(OH)2•H2O═BaCl2+2NH3↑+10H2O | |
| B. | 2HI(g)═H2(g)+I2(g)△H=+14.9 kJ.mol-1 | |
| C. | 形成化学键时共放出能量862 kJ的化学反应 | |
| D. | 能量变化如图所示的化学反应 |
分析 根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),C或氢气做还原剂时的反应.
解答 解:A.氯化铵和氢氧化钡晶体常温下反应属于吸热反应,故A错误;
B.反应的焓变为正值属于吸热反应,故B错误;
C.化学反应能量变化由断裂化学键吸收的能量和形成化学键放出的能量决定,形成化学键时共放出能量862 kJ的化学反应可能是吸热反应,故C错误;
D.图象中反应物能量高于生成物,反应一定是放热反应,故D正确;
故选D.
点评 本题考查了放热反应的判断,难度不大,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.25℃时,三种酸的电离平衡常数如下:
回答下列问题:
(1)下列四种离子结合质子的能力由大到小的顺序是a>b>d>c(填序号).
a.CO32-b.ClO-c.CH3COO-d.HCO3-
(2)下列反应不能发生的是c、d(填序号).
a.CO32-+CH3COOH=CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO32-+2HClO=CO2↑+H2O+2CO-
d.2ClO-+CO2+H2O=CO32-+2HClO
(3)用蒸馏水稀释0.10mol•L-1的醋酸,则下列各式表示的数值随水量的增加而增大的是b(填序号).
a.$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$ b.$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$ c.$\frac{c({H}^{+})}{{K}_{W}}$ d.$\frac{c({H}^{+})}{c(O{H}^{-})}$
(4)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图1,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”,下同)醋酸的平衡常数,稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液中水电离出来的c(H+).
(5)向20mL硫酸和盐酸的混合液中,逐滴加入0.05mol•L-1Ba(OH)2溶液时,生成沉淀的质量变化及由此而引起的溶液的pH的变化如图2所示.
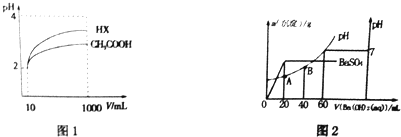
计算:①原混合溶液中c(H+)=0.3mol•L-1;c(Cl-)=0.2mol•L-1;
②A点的pH=1.
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
(1)下列四种离子结合质子的能力由大到小的顺序是a>b>d>c(填序号).
a.CO32-b.ClO-c.CH3COO-d.HCO3-
(2)下列反应不能发生的是c、d(填序号).
a.CO32-+CH3COOH=CH3COO-+CO2↑+H2O
b.ClO-+CH3COOH=CH3COO-+HClO
c.CO32-+2HClO=CO2↑+H2O+2CO-
d.2ClO-+CO2+H2O=CO32-+2HClO
(3)用蒸馏水稀释0.10mol•L-1的醋酸,则下列各式表示的数值随水量的增加而增大的是b(填序号).
a.$\frac{c(C{H}_{3}COOH)}{c({H}^{+})}$ b.$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$ c.$\frac{c({H}^{+})}{{K}_{W}}$ d.$\frac{c({H}^{+})}{c(O{H}^{-})}$
(4)体积为10mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图1,则HX的电离平衡常数大于(填“大于”、“等于”或“小于”,下同)醋酸的平衡常数,稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液中水电离出来的c(H+).
(5)向20mL硫酸和盐酸的混合液中,逐滴加入0.05mol•L-1Ba(OH)2溶液时,生成沉淀的质量变化及由此而引起的溶液的pH的变化如图2所示.

计算:①原混合溶液中c(H+)=0.3mol•L-1;c(Cl-)=0.2mol•L-1;
②A点的pH=1.
17.下列有机物的系统命名中正确的是( )
| A. | 3-甲基-4-乙基戊烷 | B. | 3,4,4-三甲基己烷 | ||
| C. | 3-甲基-5-己烯 | D. | 3,3-二甲基-1-戊烯 |
14.实验测得常温下0.1mol/L某一元酸HA溶液的pH≠1,0.1mol/L某一元碱BOH溶液里$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12.将此两种溶液等体积混合后,所得溶液呈的各离子浓度间关系正确的是( )
| A. | c (A-)>c (B+)>c (H+)>c (OH-) | B. | c (B+)=c (A-)>c (H+)=c (OH-) | ||
| C. | c (OH-)-c (H+)=c(HA) | D. | c (B+)+c (H+)=c (A-)+c (OH-)+c(HA) |
1.关于酶的说法中不正确的是( )
| A. | 酶是蛋白质 | B. | 酶是激素 | ||
| C. | 酶是催化剂 | D. | 酶是高分子化合物 |
18.氢气是人类最理想的能源.已知在25℃、101kPa下,1g氢气完全燃烧生成液态水时放出热量142.9kJ,今有如下三个热化学方程式:
(1)H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H1=akJ/mol
(2)2H2(g)+O2(g)═2H2O(l)△H2=bkJ/mol
(3)H2O(l)═H2(g)+$\frac{1}{2}$O2(g)△H3=ckJ/mol
下列关于它们的表述正确的是( )
(1)H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H1=akJ/mol
(2)2H2(g)+O2(g)═2H2O(l)△H2=bkJ/mol
(3)H2O(l)═H2(g)+$\frac{1}{2}$O2(g)△H3=ckJ/mol
下列关于它们的表述正确的是( )
| A. | 2c=b | B. | c=+285.8 | ||
| C. | 通过原电池可以实现反应(3) | D. | 氢气的燃烧热为a kJ/mol |
19.化学概念在逻辑上存在如下关系:
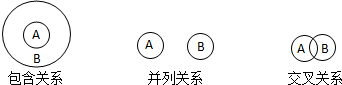
对下列概念的说法正确的是( )

对下列概念的说法正确的是( )
| A. | 纯净物与混合物属于包含关系 | |
| B. | 胶体与分散系属于交叉关系 | |
| C. | 置换反应与离子反应属于交叉关系 | |
| D. | 氧化还原反应与分解反应属于并列关系 |
 随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视.
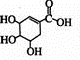 +Br2→
+Br2→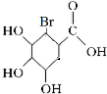 .
.