题目内容
X,Y,Z三种气体,把a molX和b molY充入一密闭容器中,发生反应:X+2Y?2Z 达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为( )A.

B.
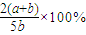
C.

D.
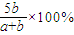
【答案】分析:令参加反应的Y的物质的量为nmol,利用三段式用n表示平衡时各组分的物质的量,再根据n(X)+n(Y)=n(Z)列方程计算n的值,根据转化率定义计算.
解答:解:令参加反应的Y的物质的量为nmol,则:
X+2Y?2Z
开始(mol):a b 0
变化(mol):0.5n n n
平衡(mol):a-0.5n b-n n
故a-0.5n+b-n=n
解得n=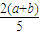 mol,故Y的转化率=
mol,故Y的转化率=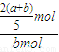 ×100%=
×100%=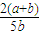 ×100%,
×100%,
故选B.
点评:本题考查化学平衡的有关计算,难度不大,注意利用三段式解题法进行的解答.
解答:解:令参加反应的Y的物质的量为nmol,则:
X+2Y?2Z
开始(mol):a b 0
变化(mol):0.5n n n
平衡(mol):a-0.5n b-n n
故a-0.5n+b-n=n
解得n=
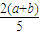 mol,故Y的转化率=
mol,故Y的转化率=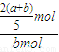 ×100%=
×100%=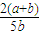 ×100%,
×100%,故选B.
点评:本题考查化学平衡的有关计算,难度不大,注意利用三段式解题法进行的解答.

练习册系列答案
相关题目

 一定温度下,在2L的密闭容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,依据题意,回答下列问题.(1)反应开始到10s,用Z表示的反应速率为
一定温度下,在2L的密闭容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,依据题意,回答下列问题.(1)反应开始到10s,用Z表示的反应速率为 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列说法正确的是( )
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示.下列说法正确的是( )