题目内容
11.在一定温度下,将0.2mol的碘化氢充入1L的密闭容器中,充分反应,达到平衡后,测得c(H2)=0.08mol/L.(1)求该反应的平衡常数.
(2)在上述温度下,该容器中若充入碘化氢0.4mol,求达到平衡时碘化氢的转化率和氢气的物质的量浓度.
分析 达到平衡时,测得c(H2)=0.08mol/L,则 2HI(g)?H2(g)+I2(g)
起始时各物质的浓度(mol•L-1) 0.2 0 0
各物质的浓度变化量(mol•L-1) 0.16 0.08 0.08
平衡时各物质的浓度(mol•L-1) 0.04 0.08 0.08
(1)利用平衡的浓度计算K,K为生成物浓度幂之积与反应物浓度幂之积的比;
(2)设转化的碘化氢为x,利用三段法得出各物质的平衡浓度,平衡常数与(1)相同,以此来计算.
解答 解:达到平衡时,测得c(H2)=0.08mol/L,则 2HI(g)?H2(g)+I2(g)
起始时各物质的浓度(mol•L-1) 0.2 0 0
各物质的浓度变化量(mol•L-1) 0.16 0.08 0.08
平衡时各物质的浓度(mol•L-1) 0.04 0.08 0.08
(1)平衡时c(H2)=c(I2)=0.08mol/L,c(HI)=0.04mol/L,
则K=$\frac{0.08×0.08}{0.04{\;}^{2}}$=4,
答:该反应的平衡常数为4;
(2)在上述温度下,该容器中若充入碘化氢0.4mol,设HI转化了x
则 2HI(g)?H2(g)+I2(g)
起始时各物质的浓度(mol•L-1) 0.4 0 0
各物质的浓度变化量(mol•L-1) x 0.5x 0.5x
平衡时各物质的浓度(mol•L-1) 0.4-x 0.5x 0.5x
K=$\frac{0.5x×0.5x}{(0.4-x){\;}^{2}}$=4,
解得:x=0.32 mol;
碘化氢转化率=$\frac{0.32mol}{0.4mol}$×100%=80%
所以平衡时c(H2)=$\frac{0.5×0.32mol}{1L}$=0.16mol/L;
答:平衡时碘化氢的转化率为80%,氢气的物质的量浓度为0.16mol/L.
点评 本题考查化学平衡的计算,明确化学平衡的三段法计算格式及平衡常数的计算方法是解答本题的关键,注意利用平衡浓度计算平衡常数,题目难度中等.

| A. | NaCl晶体 | B. | 液态氯化氢 | C. | 熔融的KNO3 | D. | NH3•H2O |
| A. | 熔融的NaCl | B. | KNO3溶液 | C. | Cu | D. | 酒精 |
| A. | Cl2 | B. | SO2 | C. | NH3 | D. | O2 |
| A. | Na | B. | FeCl3溶液 | C. | KMnO4酸性溶液 | D. | 溴水 |
| A. | HCOOH+H2O?HCOO-+H3O+ | B. | CO32-+H2O?HCO3-+OH- | ||
| C. | CO2+H2O?HCO3-+H+ | D. | HS-?S2-+H+ |

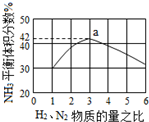 氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,氨是最重要的氮肥,是产量最大的化工产品之一.其工业合成原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.在密闭容器中,使2mol N2和6mol H2混合发生以上反应.
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,氨是最重要的氮肥,是产量最大的化工产品之一.其工业合成原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.在密闭容器中,使2mol N2和6mol H2混合发生以上反应.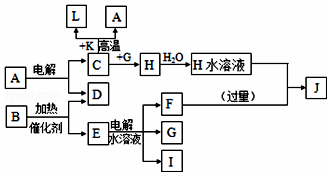 已知C、D、G、I为短周期元素形成的单质,D、G、I常温下为气态,且G为黄绿色;形成D的元素原子的最外层电子数是次外层的3倍;B的焰色反应呈紫色(透过蓝色钴玻璃);K为红棕色粉末.其转化关系如图:
已知C、D、G、I为短周期元素形成的单质,D、G、I常温下为气态,且G为黄绿色;形成D的元素原子的最外层电子数是次外层的3倍;B的焰色反应呈紫色(透过蓝色钴玻璃);K为红棕色粉末.其转化关系如图: