题目内容
3.ClO2与Cl2的氧化性相近,常温下均为气体,在自来水消毒和果蔬保鲜等方面应用广泛.某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究.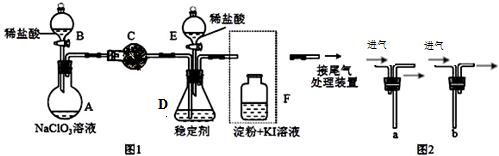
(1)仪器C的名称是:球形干燥管.安装F中导管时,应选用图2中的:b.(填“a”或“b”)
(2)打开B的活塞,A中氯酸钠和稀盐酸混和产生Cl2和ClO2,写出反应化学方程式:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O;为使ClO2在D中被稳定剂充分吸收,可采取的措施是:调节分液漏斗B的旋塞,减缓(慢)稀盐酸滴加速度.
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是:吸收Cl2.
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为:4H++5ClO2?═Cl?+4ClO2↑+2H2O,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是:检验是否有ClO2生成.
(5)已吸收ClO2气体的稳定剂Ⅰ和Ⅱ,加酸后释
放ClO2的浓度随时间的变化如图3所示,若将其用于
水果保鲜,你认为效果较好的稳定剂的原因是稳定剂II可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度.

分析 (1)根据仪器特征,可知仪器C是球形干燥管;F装置应是Cl2和KI反应,还需要连接尾气处理装置,所以应长管进气,短管出气;
(2)根据电子转移守恒和原子守恒书写氯酸钠和稀盐酸混和产生Cl2和ClO2的反应化学方程式,为使ClO2在D中被稳定剂充分吸收,产生ClO2的速率要慢;
(3)F装置中发生Cl2+2KI=2KCl+I2时,碘遇淀粉变蓝,而F中溶液的颜色不变,说明Cl2被吸收;
(4)在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,根据元素守恒可知应还有水生成,该反应的离子方程式为4H++5ClO2-=Cl-+4ClO2↑+2H2O; 在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是验证是否有ClO2 生成;
(5)由图可知,稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度.
解答 解:(1)根据仪器特征,可知仪器C是球形干燥管;F装置应是Cl2和KI反应,还需要连接尾气处理装置,所以应长管进气,短管出气,故选b,
故答案为:锥形瓶;b;
(2)氯酸钠和稀盐酸混和产生Cl2和ClO2,NaClO3中氯为+5价被还原成ClO2中+4价,盐酸中氯为-1价,被氧化成0价氯,转移电子数为2,所以NaClO3、ClO2前系数为2,Cl2前系数为1,反应化学方程式:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O,:为使ClO2在D中被稳定剂充分吸收,产生ClO2的速率要慢,故滴加稀盐酸的速度要慢,即调节分液漏斗B的旋塞,减缓(慢)稀盐酸滴加速度,
故答案为:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O;调节分液漏斗B的旋塞,减缓(慢)稀盐酸滴加速度;
(3)F装置中发生Cl2+2KI=2KCl+I2时,碘遇淀粉变蓝,而F中溶液的颜色不变,则装置C的作用是吸收Cl2,
故答案为:吸收Cl2;
(4)在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,根据元素守恒可知应还有水生成,该反应的离子方程式为:4H++5ClO2-=Cl-+4ClO2↑+2H2O; 在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是验证是否有ClO2 生成,
故答案为:4H++5ClO2-=Cl-+4ClO2↑+2H2O;检验是否有ClO2生成;
(5)由图可知,稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度,所以稳定剂Ⅱ好,
故答案为:稳定剂Ⅱ可以缓慢释放ClO2,能较长时间维持保鲜所需的浓度.
点评 本题以ClO2的制备、吸收、释放为载体,考查实验制备方案设计、基本操作、对装置及操作的分析评价等,注意根据问题进行制备流程分析,题目难度中等.

(1)硝酸尾气吸收法是利用碱溶液吸收汽车尾气,该方法的优点是对尾气进行回收利用,减小污染.
(2)使用复分解法制备硝酸钠的流程如下:

①反应器和除钙器中发生反应的化学方程式分别为:Ca(NO3)2+Na2SO4=CaSO4↓+2NaNO3;Na2CO3+Ca(NO3)2=CaCO3↓+2NaNO3.
②酸化槽中,应加硝酸调节pH=7,才能使杂质除去,又减少硝酸的浪费;为提高酸化除杂的效率,除了适当提高硝酸浓度外,还可以采取的措施是可以搅拌、适当升高温度.
③研究生产过程中水、硫酸钠、碳酸钠的用量与硝酸钠浸出率之间的关系,其中水加入量对硝酸钠浸出率的影响的实验结果见下表:
| 水/硝酸钙 | 0.8:1 | 0.9:1 | 0.95:1 | 1:1 | 1.05:1 | 1.1:1 | 1.15:1 |
| 浸出率/% | 83.1 | 94.5 | 98.2 | 99.1 | 99.5 | 99.6 | 99.7 |
(3)用硝酸钠、木炭、硫磺也可以制得威力巨大的火药,爆炸时产生一种单质,一种氧化物以及一种金属硫化物,其中,除硝酸钠之外,另外一种氧化剂和还原剂的比为1:3,请写出该反应的方程式2NaNO3+S+3C=Na2S+N2↑+3CO2↑,.
(4)硝酸钠在加热条件下发生分解产生亚硝酸钠(NaNO2),某同学进行该实验得到粗产品,取2.000g产品配成l00.00mL溶液,取25.00mL溶液,用0.l000mol/L的酸性高锰酸钾溶液进行滴定,重复实验4次,平均消耗酸性高锰酸钾溶液的体积为19.50mL,则粗产品中亚硝酸钠的质量百分含量为为67.27%.
(摩尔质量:NaNO2-69g/mol)
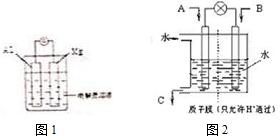 电能与化学能之间的转化具有重要的使用价值.
电能与化学能之间的转化具有重要的使用价值.