题目内容
3.下列叙述正确的是( )| A. | 漂白粉、次氯酸溶液和明矾都是混合物 | |
| B. | 不能通过化合反应制得FeCl2和Fe(OH)3 | |
| C. | 铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧 | |
| D. | 用强光照射装满次氯酸的试管(倒置于水槽中)可收集到两种气体 |
分析 A.漂白粉的主要成分为氯化钙、次氯酸钙,次氯酸溶液为HClO和水的混合物,明矾为十二水硫酸铝钾;
B.Fe与氯化铁反应生成氯化亚铁,氢氧化亚铁、氧气和水化合生成氢氧化铁;
C.Fe与氧气反应生成四氧化三铁,Fe与水蒸气高温下发生氧化还原反应生成四氧化三铁和氢气;
D.HClO光照分解生成氧气.
解答 解:A.漂白粉的主要成分为氯化钙、次氯酸钙,次氯酸溶液为HClO和水的混合物,明矾为十二水硫酸铝钾,则明矾为化合物,故A错误;
B.Fe与氯化铁反应生成氯化亚铁,氢氧化亚铁、氧气和水化合生成氢氧化铁,则能通过化合反应制得FeCl2和Fe(OH)3,故B错误;
C.Fe与氧气反应生成四氧化三铁,Fe与水蒸气高温下发生氧化还原反应生成四氧化三铁和氢气,则铁能在氧气中剧烈燃烧,但不能在水蒸气中燃烧,故C正确;
D.HClO光照分解生成氧气,则用强光照射装满次氯酸的试管(倒置于水槽中)可收集到一种气体,故D错误;
故选C.
点评 本题考查物质的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,注意元素化合物知识的综合应用,题目难度不大.

练习册系列答案
相关题目
11.将pH=8的氢氧化钠溶液和pH=10的氢氧化钠溶液等体积混合后,溶液中的C(H+)最接近( )
| A. | $\frac{{{{10}^{-8}}+{{10}^{-10}}}}{2}mol/L$ | B. | $\frac{{{{10}^{-6}}+{{10}^{-4}}}}{2}mol/L$ | ||
| C. | (10-8+10-10)mol/L | D. | 2×10-10mol/L |
12.某原电池反应的离子方程式为Zn+Cu2+═Zn2++Cu,关于此原电池,下列说法中正确的是( )
| A. | Cu(NO3)2溶液可作电解质溶液 | |
| B. | 在电解质溶液中,电子由负极流向正极 | |
| C. | 锌极的质量先减小后增大 | |
| D. | 可用镁作正极材料 |
8.下列说法不正确的是( )
| A. | 油脂水解的产物是高级脂肪酸和丙三醇 | |
| B. | 油脂属于混合物 | |
| C. | 油脂、乙醇是人体必需的营养物质 | |
| D. | 水果因含有酯类物质而具有香味 |
12.非金属元素H、C、O、S、Cl能形成的化合物种类很多,单质及化合物的用途很广泛.
(1)O2-的电子式为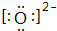 ;
;
(2)O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例O3、Cl2(写化学式,任写两种);
(3)CH3OH在常温下为液态,沸点高于乙烷的主要原因是甲醇分子之间能形成氢键,而乙烷不能;
(4)Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
①用离子方程式表示“泄漏处理”中NaHSO3溶液的作用HSO3-+Cl2+H2O=SO42-+3H++2Cl-.
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是Fe(或者FeCl3)能催化苯与氯气的反应.
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3.当溶液中c(Cl-):c(ClO-)=11:1时,则c(ClO-):c(ClO3-)比值等于1:2.
(5)镁是一种较活泼的金属,Mg与Ca类似,也能与C形成某种易水解的离子化合物.已知该化合物0.1mol与水完全反应后,产生0.1mol的某种气体.该气体被溴水全部吸收后,溴水增重2.6g.请写出该水解反应方程式MgC2+2H2O=Mg(OH)2+C2H2↑.
(1)O2-的电子式为
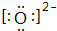 ;
;(2)O、Cl两元素形成的单质和化合物常用来杀菌消毒,试举例O3、Cl2(写化学式,任写两种);
(3)CH3OH在常温下为液态,沸点高于乙烷的主要原因是甲醇分子之间能形成氢键,而乙烷不能;
(4)Cl2是一种大气污染物,液氯储存区贴有的说明卡如下(部分):
| 危险性 |  |
| 储运要求 | 远离金属粉末、氨、烃类、醇类物质;设置氯气检测仪 |
| 泄漏处理 | NaOH、NaHSO3溶液吸收 |
| 包装 | 钢瓶 |
②若液氯泄漏后遇到苯,在钢瓶表面氯与苯的反应明显加快,原因是Fe(或者FeCl3)能催化苯与氯气的反应.
③将Cl2通入适量KOH溶液中,产物中可能有KCl、KClO、KClO3.当溶液中c(Cl-):c(ClO-)=11:1时,则c(ClO-):c(ClO3-)比值等于1:2.
(5)镁是一种较活泼的金属,Mg与Ca类似,也能与C形成某种易水解的离子化合物.已知该化合物0.1mol与水完全反应后,产生0.1mol的某种气体.该气体被溴水全部吸收后,溴水增重2.6g.请写出该水解反应方程式MgC2+2H2O=Mg(OH)2+C2H2↑.


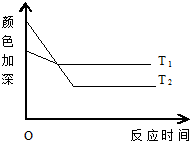 反应A+B?2C,其中A为有色气态物质,其混合物颜色深浅与反应时间、温度(t)之间的关系如图所示(B、C均为无色物质):
反应A+B?2C,其中A为有色气态物质,其混合物颜色深浅与反应时间、温度(t)之间的关系如图所示(B、C均为无色物质):