题目内容
8.具有下列电子排布式的原子中,半径最小的是( )| A. | ls22s22p63s23p3 | B. | 1s22s22p3 | C. | 1s22s2sp4 | D. | 1s22s22p63s23p4 |
分析 原子的电子层数越多,其原子半径越大,相同电子层数的原子,原子半径随着原子序数的增大而减小,据此分析解答.
解答 解:原子的电子层数越多,其原子半径越大,相同电子层数的原子,原子半径随着原子序数的增大而减小,
根据原子核外电子排布式知,B、C电子层数都是2,A、D电子层数都是3,所以A和D的原子半径大于B和C,
C的原子序数为大于B,属于同一周期元素,同一周期元素,原子半径随着原子序数的增大而减小,所以C的原子半径小于B,则原子半径最小的是C,
故选C.
点评 本题考查了原子半径大小的判断,明确原子半径与电子层数、原子序数(相同电子层数)之间的关系即可解答,难度不大.

练习册系列答案
相关题目
3.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 0.3 mol•L-1 的NH4NO3溶液中含有的NO-3数目为0.3NA | |
| B. | 常温常压下,5.6gC2H4和C3H6的混合气体中含氢原子数为0.9NA | |
| C. | 将标准状况下11.2L的Cl2通入足量水中,转移的电子总数为0.5NA | |
| D. | 一定量的Fe与含1 mol HNO3的稀硝酸恰好反应,则被还原的氮原子数小于NA |
13.下列变化中,需加入还原剂的是( )
| A. | SO32-→SO2 | B. | S2-→S | C. | AlO2-→Al3+ | D. | CO2→CO |
20.下列关于热化学反应的描述中正确的是( )
| A. | HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的反应热△H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+566.0 kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
17.下列反应的离子方程式书写正确的是( )
| A. | 含等物质的量的MgCl2、Ba(OH)2、HNO3三种溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| B. | CaCO3溶于CH3COOH:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 过量HI溶液加入到Fe(NO3)3溶液中:2Fe3++2I-═2Fe2++I2 | |
| D. | 向NaClO溶液中通入少量SO2:3ClO-+SO2+H2O═2HClO+SO42-+Cl- |
18.下列化学反应的离子方程式正确的是( )
| A. | Cu溶于稀硝酸:Cu+2H++NO3-═Cu2++NO2+H2O | |
| B. | NaAl02溶液中通入过量CO2气体:AlO2-+CO2+2H2O═Al(OH)3+HCO3- | |
| C. | 用CH3COOH溶解CaCO3:CaC03+2H+═Ca2++H2O+CO2 | |
| D. | NH4 HCO3溶液与足量的NaOH溶液反应:HCO3-+OH-═CO32-+H2O |
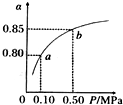 已知2A(g)+B(g)?2C(g),向容积为1L的密闭容器中加入0.50mol A和0.25mol B,在500℃时充分反应,达平衡后测得c(C)=0.4mol•L-1,放出热量Q1 kJ.
已知2A(g)+B(g)?2C(g),向容积为1L的密闭容器中加入0.50mol A和0.25mol B,在500℃时充分反应,达平衡后测得c(C)=0.4mol•L-1,放出热量Q1 kJ.