题目内容
几种短周期元素的原子半径及主要化合价如表:下列叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6、-2 | +2 | -2 |
| A、L、M的单质与稀硫酸反应速率:M>L |
| B、T、Q的氢化物常态下均为无色气体 |
| C、R是非金属元素 |
| D、M3+是同周期简单离子中半径最小的 |
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:在主族元素中,元素的最高化合价与其族序数相等,原子的电子层数越多其原子半径越大,根据元素化合价知,L、R属于第IIA元素,L的原子半径大于R,则L是Mg元素、R是Be元素;
M属于第IIIA族元素,M原子半径大于R,所以M是Al元素;
Q最高化合价是+6价,最低负价是-2价,则Q是S元素;
T元素最低负价是-2价,则T是O元素,再结合物质结构、性质解答.
M属于第IIIA族元素,M原子半径大于R,所以M是Al元素;
Q最高化合价是+6价,最低负价是-2价,则Q是S元素;
T元素最低负价是-2价,则T是O元素,再结合物质结构、性质解答.
解答:
解:在主族元素中,元素的最高化合价与其族序数相等,原子的电子层数越多其原子半径越大,根据元素化合价知,L、R属于第IIA元素,L的原子半径大于R,则L是Mg元素、R是Be元素;M属于第IIIA族元素,M原子半径大于R,所以M是Al元素;Q最高化合价是+6价,最低负价是-2价,则Q是S元素;T元素最低负价是-2价,则T是O元素,
A.L为Mg、M为Al元素,Mg的金属性大于Al,所以L、M的单质与稀硫酸反应速率:M<L,故A错误;
B.T为O元素、Q为S元素,常态下水是液体,故B错误;
C.R为Be元素,Be单质为金属,B为金属元素,故C错误;
D.M为Al,M3+为铝离子,铝为第三周期元素,第三周期中的非金属离子半径大于金属离子,金属离子中,金属中核电荷数最大的为铝,则第三周期的金属离子中铝离子为半径最小的,所以铝离子为第三周期的离子中离子半径最小的离子,故D正确;
故选D.
A.L为Mg、M为Al元素,Mg的金属性大于Al,所以L、M的单质与稀硫酸反应速率:M<L,故A错误;
B.T为O元素、Q为S元素,常态下水是液体,故B错误;
C.R为Be元素,Be单质为金属,B为金属元素,故C错误;
D.M为Al,M3+为铝离子,铝为第三周期元素,第三周期中的非金属离子半径大于金属离子,金属离子中,金属中核电荷数最大的为铝,则第三周期的金属离子中铝离子为半径最小的,所以铝离子为第三周期的离子中离子半径最小的离子,故D正确;
故选D.
点评:本题考查了原子结构和元素性质,明确元素化合价、原子半径与原子结构和元素族序数之间的关系即可解答,注意A选项可以根据对角线规则分析,题目难度中等.

练习册系列答案
相关题目
无机化学命名委员会(国际组织)在1989年作出决定,把长式元素周期表原先的主、副族 及族号取消,由左到右改为18列,如碱金属族为第1列,稀有气体元素为第18列.按此规定,下列说法中错误的是( )
| A、第17、18列都是非金属元素 |
| B、第1列元素和第17列元素的单质熔、沸点变化趋势相反 |
| C、只有第2列元素原子最外层有2个电子 |
| D、在18列元素中,第3列元素种类最多 |
柠檬烯是一种食用香料,其结构简式如图.有关柠檬烯的分析正确的是( )
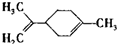

| A、它的一氯代物有6种 |
B、它和丁基苯(  )互为同分异构体 )互为同分异构体 |
| C、一定条件下,它分别可以发生加成、取代、氧化等反应 |
| D、它的分子中所有的碳原子一定在同一个平面上 |